![]()
![]()
![]()
![]()
![]()
 |
 |
|
|

![]()
![]()
Invitado # 36 : (Noviembre 2003)
"Cicatrización de los procedimientos quirúrgicos en endodoncia
por Alessandra Alvarado Masó
Odontólogo, Universidad Central de Venezuela, 1999
Especialista en Endodoncia, U.C.V., Venezuela, 2001-2002
e-mail: alealvaradomaso@cantv.net
Resumen
El clínico que realiza un procedimiento quirúrgico endodóntico se enfrenta a diversas variables que exigen un profundo conocimiento de las estructuras anatómicas, técnicas quirúrgicas, materiales y proceso de cicatrización de los tejidos. En esta revisión de la literatura, se podrá encontrar información referente a las estructuras anatómicas sanas que están involucradas en un procedimiento quirúrgico endodóntico y las generalidades del proceso de cicatrización de los tejidos. Seguidamente, se hará referencia al proceso de cicatrización de los tejidos blandos, periapicales y radiculares después de una resección apical, resección apical y obturación a retro, reimplante intencional, regeneración tisular guiada e implante óseo. Para concluir, al final de la revisión, se hará alusión a diversos artículos publicados que sirven como guía para la determinación de la cicatrización después de un procedimiento quirúrgico endodóntico.
Introducción
La cicatrización de los tejidos blandos, periapicales y radiculares, involucra una serie de mecanismos y eventos biológicos complejos que pueden ocurrir simultáneamente o no. Así mismo, la cicatrización dependerá del tipo de tejido lesionado y la clase de herida realizada, es por esto que la respuesta de cicatrización en una cirugía perirradicular es diversa y complicada.
Durante el proceso de cicatrización algunos tejidos cicatrizan por primera intención y sufren una completa regeneración, otros por el contrario lo hacen por segunda intención, lo que trae como consecuencia la reparación de la herida.
El objetivo principal del acto quirúrgico endodóntico, es la eliminación del factor etiológico para permitir la cicatrización de los tejidos periapicales; idealmente lo que se quiere lograr es la completa regeneración de estas estructuras.
El conocimiento del proceso de cicatrización de los diferentes tejidos involucrados en una cirugía periapical, es esencial para poder determinar si hubo o no reparación o regeneración y por lo tanto establecer el pronóstico del caso.
No cabe duda de que la evaluación histológica de los tejidos periapicales, nos proporciona la mejor información acerca de la condición periapical después de una cirugía endodóntica. Desafortunadamente este método de evaluación no puede ser utilizado y por lo tanto la evaluación debe basarse en los hallazgos clínicos y radiográficos.
Aunque se ha podido demostrar en diversos estudios que no existe correlación exacta entre la condición histológica y los hallazgos clínicos y radiográficos, actualmente son la única herramienta disponible.
Después de realizar un procedimiento quirúrgico endodóntico sería excelente poder realizar controles postoperatorios clínicos y radiográficos por varios años, para poder determinar si el caso cicatrizó completamente, incompletamente, inciertamente o insatisfactoriamente y de esta forma establecer el pronóstico y tratamiento adecuado.
El presente trabajo tiene por objetivo analizar el proceso de cicatrización de los tejidos después de realizar un procedimiento quirúrgico endodóntico.
Características del Periodonto de Protección y de Inserción. Generalidades
El periodonto se divide de acuerdo a su función en: periodonto de protección y de inserción. 1 El de protección está compuesto por la encía que es la parte de la mucosa bucal masticatoria que tapiza los procesos alveolares y rodea al cuello de los dientes; 1,2 y la unión dentogingival que une la encía al diente. 1 Embriológicamente estas estructuras derivan del ectodermo superficial, específicamente del epitelio de la mucosa bucal.3,4
Mientras que el periodonto de inserción está compuesto por tres estructuras: cemento, ligamento periodontal y hueso alveolar 5,6 (Gráficos 1 y 2). Estas tres estructuras derivan del ectomesénquima cefálico, específicamente del saco dental.3 Las fibras colágenas del ligamento periodontal se insertan al cemento radicular por un lado, y por el otro, al hueso que rodea el alvéolo,2,5,6 constituyendo la articulación alvéolodentaria que permite que el diente se mantenga en su posición y resista las fuerzas masticatorias.2,5
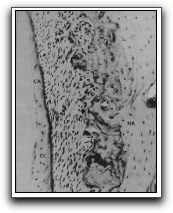 |
Gráfico 1. Periodonto de inserción. Se observa cemento acelular (CA), cemento celular (CC), ligamento periodontal (LP), hueso alveolar (HA). Tomado de Gómez y Campos. 1999. |
 |
|
|
Gráfico 2. Detalle de la zona superior (próximo a cervical) del periodonto de inserción de un diente prefuncional. Se observa una capa delgada de cemento; la membrana periodontal y la compacta periodóntica o lámina cribosa del hueso alveolar. Técnica por descalcificación, x 60.Tomado de Gómez y Campos. 1999. |
Características clínicas e histológicas de la encía: La encía es esa parte de la mucosa masticatoria que recubre la apófisis alveolar y rodea la porción cervical de los dientes.2,4 La misma se divide en dos regiones: la encía libre o marginal, y la encía fija o adherida.1,2,4,7
La encía libre constituye la región de la mucosa que no está unida al hueso subyacente y que se extiende desde el borde gingival libre hasta el surco gingival marginal.1,4,7 Por lo general mide 1 mm de ancho y puede separarse de la superficie dental mediante una sonda periodontal.2 La encía adherida, unida al periostio del hueso alveolar, es la continuación apical de la encía libre; ésta se extiende desde el surco libre gingival hasta la unión del surco mucogingival.1,2,4,7
La encía que se extiende entre diente y diente forma la papila interdental, que posee forma piramidal en la zona anterior y es aplanada en la zona posterior,1,4 la papila interdental se adapta a la morfología del contacto interproximal, 2 (Gráficos 3, 4, 5 y 6).
En cuanto a las características clínicas, si la encía se encuentra en condiciones de salud, la encía libre es de color rosado coral, de superficie lisa, brillante, de consistencia blanda y móvil.1,4 Terminada la erupción dentaria, el margen gingival libre se ubica sobre la superficie adamantina aproximadamente 0,5-2 mm hacia coronario del límite cemento-esmalte.4
 |
|
|
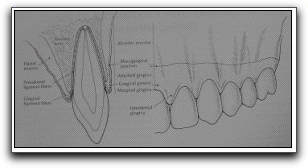
Gráfico 3. Tejidos duros y blandos que constituyen al periodonto. Tomado de Gutmann y Harrison. 1994. |
 |
|
|
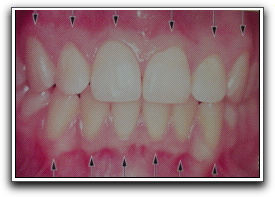
Gráfico 4. La encía. En sentido coronario, la encía rosada coral termina en el margen gingival libre, que tiene un contorno festoneado. En sentido apical, la encía se continúa con la mucosa alveolar, laxa y roja oscura, de la cual está separada por lo que es, habitualmente, un límite fácil de reconocer llamado límite mucogingival (flechas). Tomado de Lindhe. 2000. |
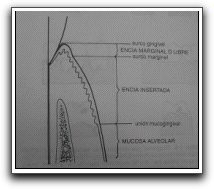 |
Gráfico 5. Diagrama que muestra los puntos anatómicos de referencia de la encía. Tomado de Carranza y Newman 1998. |
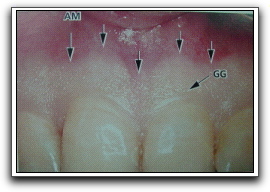 |
Gráfico 6. La encía adherida, en sentido coronario, está señalada por el surco gingival libre (GG) o, cuando ese surco no está presente, por un plano horizontal ubicado en el nivel del límite cementoadamantino. La encía adherida se extiende en dirección apical hacia la unión mucogingival (flechas), donde se continúa con la mucosa alveolar (tapiz) (AM). Tomado de Lindhe 2000. |
La encía adherida es de color rosado pálido, de consistencia firme y aspecto rugoso (cáscara de naranja),1,4,7 pero este puntillado no está presente en todos los individuos, solo en un 40%; actualmente se sabe que su ausencia no indica enfermedad periodontal.1,4
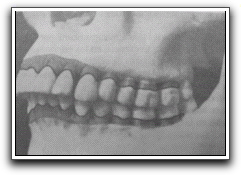
La longitud de la encía adherida puede variar de una persona a otra.2,4,7 Algunos autores refieren medidas aproximadas dependiendo del diente. Por ejemplo, la encía adherida vestibular de los incisivos y premolares superiores, mide de 8 a 10mm; en los caninos superiores tiende a ser un poco mayor. Los molares superiores, por el contrario, presentan una encía adherida de aproximadamente 5 a 6mm. En cuanto a los dientes inferiores, los incisivos, premolares y molares tienen de 6 a 8mm y los caninos de 5 a 7mm aproximadamente 8 (Gráfico 7). La cantidad de encía adherida se debe calcular antes de planificar el colgajo, para prevenir futuras complicaciones.7
 |
|
|
|
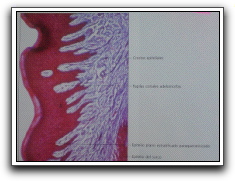
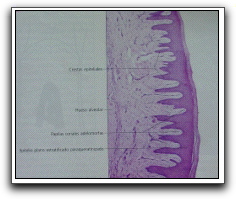
Histológicamente se definen dos zonas en la encía libre, epitelio y corion. En cuanto al epitelio, éste está conectado al tejido conjuntivo por una interface ondulada, debido a las proyecciones papilares, también se observan crestas epiteliales interpapilares. El epitelio de la encía libre puede ser de dos tipos: queratinizado o no queratinizado y se pueden apreciar cuatro capas celulares, basal, espinosa, granulosa y córnea,1,2,4 (Gráficos 8, 9, 10 y 11).
 |
|
|
|
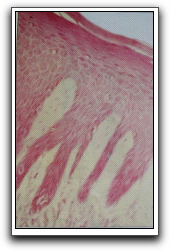 |
Gráfico 9. Encía libre, se observan las cresta epiteliales y las papilas coriales. En el extremo distal de las crestas se identifican células claras. HE, x 100. Tomado de Gómez y Campos. 1999. |
 |
 |
|
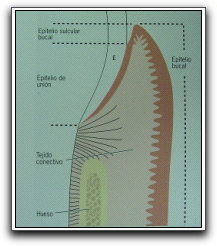
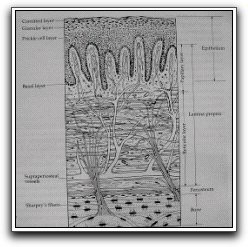
Gráfico 10. Dibujo esquemático del corte histológico (Gráfico 11), que describe la composición de la encía y el área de contacto entre la encía y el esmalte (E). Espesor medio de la encía insertada en la dentición humana permanente. Tomado de Lindhe 2000. |
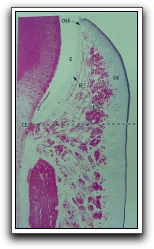
Gráfico 11. La encía libre comprende todas las estructuras tisulares ubicadas de forma coronaria a una línea horizontal ubicada en el nivel cementoadamantino (CEJ). El epitelio que recubre la encía libre puede diferenciarse así: epitelio bucal (OE), que mira hacia la cavidad bucal; epitelio del surco (OSE), que mira hacia el diente sin ponerse en contacto con él; epitelio de inserción (JE), que permite el contacto entre encía y diente. Tomado de Lindhe 2000. |
También se pueden observar melanocitos, células de Langerhans y células de Merkel; a estas células se les llaman células claras, son de forma estrellada y tienen prolongaciones citoplasmáticas de distintos tamaños y aspectos,1,4 (Gráfico 9).
El corion presenta un tejido conjuntivo semidenso que posee una cantidad similar de células y fibras. Las células que se pueden encontrar son: fibroblastos (célula predominante, alrededor del 65%), células cebadas, macrófagos, polimorfonucleares neutrófilos, linfocitos y plasmocitos.1,2,4
Además, se pueden apreciar fibras colágenas, (Gráfico 12), fibras de reticulina, (Gráfico 13), escasas fibras elásticas, fibras de elaunina y fibras de oxitalán, (Gráfico 14). Las fibras colágenas principalmente son de tipo I. La sustancia intercelular amorfa contiene glicosaminoglicanos (ácido hialurónico y condroitín sulfato) y glicoproteinas.1,2,4
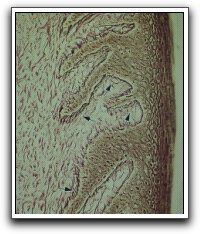
En la encía adherida el epitelio es de tipo plano estratificado queratinizado o no queratinizado1,2,4,7 y el corion es de tipo denso fibroso. Posee abundantes papilas delomorfas que dan un aspecto puntiforme,1 (Gráficos 15 y 16). El tejido conjuntivo que conecta a la encía libre con la adherida, posee gruesos haces de fibras colágenas que se entremezclan con las provenientes del periostio y ligamento periodontal. Éstas se disponen en una especie de anillo y es llamado ligamento gingival o supracrestal.1,7 El 30% de la encía adherida está compuesto por epitelio y el otro 70% por tejido conjuntivo.7
 |
|
|
|
 |
|
|
|
 |
|
|
|
 |
|
|
|
 |
|
|
|
Las fibras gingivales supracrestales1 o fibras del ligamento gingival,1,7 vistas vestibulolingualmente, unen a la cresta ósea y cemento supracrestal con la encía y el periostio de la encía adherida.
Se pueden distinguir 5 grupos de fibras gingivales: las fibras dentogingivales, las cuales se dirigen coronalmente desde el cemento supracrestal hacia la encía libre alrededor de toda la circunferencia del diente en forma de abanico;1,2,4,7 fibras dentoperiósticas, van desde el cemento que se encuentra por encima de la cresta ósea para unirse al periostio de la vertiente externa o superficie vestibular y lingual de la cresta alveolar.1,4,7
El tercer grupo consta de las fibras alvéologingivales que se extienden desde la cresta ósea alveolar y se insertan en la lámina propia tanto de la encía libre como de la adherida.1,4,7 Las fibras circulares rodean al diente en forma de anillo entrecruzándose con las otras fibras, ayudando a sujetar la encía libre al diente.1,2,4,7
Por último, las fibras transeptales 2,4,7 o dentodentales1 que parten desde el cemento cervical del diente, atraviesan al tejido conjuntivo de la encía interdental y se insertan en el cemento cervical del diente adyacente por encima de la cresta ósea alveolar,1,2,4,7 (Gráfico 17).
Características histológicas de la unión dento-gingival: La función de la unión dento-gingival es la de unir la encía al diente y está constituida por: el epitelio del surco, el epitelio de unión y el corion. El epitelio del surco, o vertiente dental de la encía libre, se continúa en el borde gingival con el epitelio de la encía libre y en sentido apical con el epitelio de unión sin que exista una división clara entre ambos, el epitelio del surco reviste al surco gingival,1,2 (Gráficos 18 y 19).
 |
|
|
|
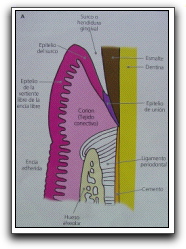 |
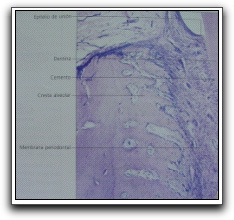
Gráfico 18. Localización de la unión dentogingival. Tomado de Gómez y Campos. 1999. |
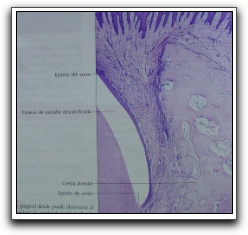 |
Gráfico 19. Sector de la región gingival donde puede observarse el epitelio del surco (corion apapilar), la unión dentogingival y la cresta alveolar. Técnica por descalcificación HE, x 60. Tomado de Gómez y Campos. 1999. |
Histológicamente este epitelio es de tipo plano estratificado no queratinizado, delgado, sin proliferaciones reticulares; semejante al epitelio de unión, aunque las células en el epitelio del surco están más próximas unas a otras y los espacios intercelulares no son tan amplios. La unión que existe entre el epitelio del surco y el tejido conjuntivo es apapilar o recta.1,2,4
El epitelio de unión suele recibir otros nombres: adherencia epitelial, epitelio de fijación, entre otros. Este epitelio une a la encía con el diente a través de una membrana basal que se extiende desde la región de la unión cemento-esmalte hasta el fondo del surco gingival, configurando un anillo alrededor del diente; de esta forma cumple con su función de protección biológica debido a que logra sellar al periodonto.1
Topográficamente tiene forma triangular de base hacia el fondo del surco gingival y vértice a nivel de la unión cemento-esmalte. Histológicamente es un epitelio plano estratificado no queratinizado,1,2 con un espesor aproximado, en el adulto, de 15 a 30 capas de células en su parte más ancha, y de 1 a 2 capas en la unión cemento-esmalte.1
La longitud del epitelio de unión varía desde 0,25 hasta 1,35mm 2. En el epitelio de unión existen dos poblaciones celulares: la primera es la población intrínseca, compuesta básicamente por queratinocitos; y la segunda, es la población extrínseca, integrada por polimorfonucleares, linfocitos y monocitos.1
El epitelio de unión y las fibras gingivales son considerados como una entidad funcional, conocida como unidad dentogingival.2
El corion del epitelio del surco y de unión, es de tipo laxo con escasos fibroblastos y fibras colágenas. En el mismo existe un infiltrado inflamatorio agudo y crónico representado por varios tipos de células, tales como: polimorfonucleares neutrófilos, linfocitos y monocitos, debido a la invasión microbiana frecuente, por lo tanto, este proceso inflamatorio se considera fisiológico.1
Características histológicas y fisiológicas del cemento: El cemento es un tejido conjuntivo mineralizado que deriva de la capa celular ectomesenquimática del folículo dentario que rodea al germen dentario. A semejanza del esmalte también recubre a la dentina, pero sólo en su porción radicular. Su función principal es anclar las fibras del ligamento periodontal a la raíz del diente, pero también controla el ancho del espacio periodontal depositándose durante toda la vida; transmite las fuerzas oclusales a la membrana periodontal; repara la superficie radicular y compensa el desgaste del diente por la atrición.4,5
Estructuralmente el cemento es comparable con el hueso debido a su dureza y composición química, pero ambos poseen características que los diferencian.4,5 El cemento radicular posee un espesor aproximado de 20 µm en la zona del cuello y de 50 a 80 µm en el tercio medio. Pero estos espesores varían con la edad, llegando a medir en la zona apical e interradicular varios milímetros.5 Otros autores reportan que puede medir desde 16 hasta 60 µm, en la mitad coronaria de la raíz y que puede alcanzar su espesor máximo en el tercio apical y las zonas de bi y trifurcación (150 a 200 µm).6
En cuanto a sus propiedades físicas, el color del cemento es más opaco que el esmalte pero menos amarillo que la dentina; su dureza es comparable a la del hueso, por lo tanto, es menor a la del esmalte y la dentina; es un tejido permeable y presenta una radiopacidad similar a la del hueso compacto.5
Estructuralmente el cemento está compuesto por cementoblastos, cementocitos y una matriz extracelular calcificada. Los cementoblastos se encargan de producir la sustancia cementoide que posteriormente (al precipitarse las sales minerales), se mineralizará. Cuando estos cementoblastos quedan atrapados en el cemento mineralizado (dentro de las lagunas), se les llama cementocitos.5,7
En cuanto a la matriz extracelular, ella contiene del 46 al 50% aproximadamente de la materia inorgánica, 22% de la materia orgánica y 5% de agua. El principal componente inorgánico es el fosfato de calcio (cristales de hidroxiapatita),4,5,6,7 la matriz orgánica está compuesta por las fibras colágenas, que en un 90% son de tipo I.5,7
El cemento radicular puede ser acelular (primario) o celular (secundario).4,5,6,7 Ambos constan de una matriz interfibrilar calcificada y fibrillas colágenas.6 El acelular se deposita lentamente antes de que el diente erupcione, por lo tanto los cementoblastos tienen tiempo para retirarse y no quedan atrapados dentro del tejido mineralizado;4,5 predominantemente este tipo de cemento, se encuentra en el tercio cervical radicular,5,6,7 pero puede cubrir la totalidad de la raíz,5 (Gráfico 20).
 |
|
|
Gráfico 20. Superficie del cemento acelular. MEB, x 2.000. Tomado de Gómez y Campos. 1999. |
Por el contrario, el cemento celular comienza a depositarse rápidamente cuando el diente entra en oclusión, y los cementoblastos quedan incluidos en la matriz calcificada (cementocitos),4,5 es más irregular y se encuentra menos calcificado que el cemento acelular.6 Generalmente este tipo de cemento se localiza en el tercio medio y apical.5,7 El cemento celular se deposita durante toda la vida compensando el desgaste oclusal de los dientes,5 (Gráfico 21).
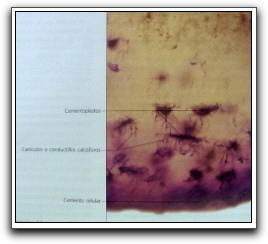 |
Gráfico 21. Detalle a mayor aumento del cemento celular. Se observa los cementoplastos y sus típicas prolongaciones. Técnica por desgaste, x 250. Tomado de Gómez y Campos. 1999. |
Características histológicas y fisiológicas del ligamento periodontal: El ligamento periodontal es el tejido conjuntivo blando, muy vascularizado y celular que rodea los dientes y une el cemento radicular con la lámina dura del hueso alveolar propio.4,6 Se continúa con el tejido conjuntivo de la encía y se comunica con los espacios medulares a través de los conductos vasculares del hueso.6
El ligamento periodontal también es conocido con los nombres de: periodonto, gonfosis, membrana periodontal, ligamento alvéolodental y desmodonto, entre muchos otros.5,7 Consiste en una delgada capa de tejido conjuntivo fibroso que a través de sus fibras une la estructura dentaria al hueso alveolar, (Gráfico 22). Su función principal es mantener al diente suspendido en su alvéolo, soportar y resistir las fuerzas de la masticación y actuar como receptor sensorial.4,5,6
En una radiografía el ligamento periodontal está incluido en el espacio entre las raíces de los dientes y la lámina dura o hueso alveolar propio.4 El ligamento periodontal en la zona apical se relaciona con el tejido pulpar y a nivel coronario se correlaciona con el corion gingival.5 El espesor del ligamento varía notablemente de un individuo a otro, depende del diente, de la zona, la función y la edad; pero por lo general se acepta que el ligamento periodontal tiene un espesor promedio de 0,10 y 0,38 µm 5 ó 0,25mm + 50%.4
 |
|
|
|
El ligamento periodontal proviene del tejido mesenquimático del saco dentario y estructuralmente, al ser un tejido conjuntivo denso presenta, células, fibras, sustancia fundamental amorfa, vasos y nervios. Las células predominantes son los fibroblastos, que representan el 20% del total de la población celular; pero también podemos observar osteoblastos, cementoblastos, osteoclastos, cementoclastos, macrófagos, mastocitos, eosinófilos, células epiteliales de Malassez, células nerviosas y células madres ectomesenquimatosas.4,5,6,7
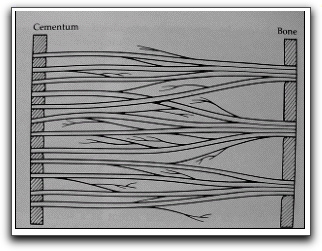
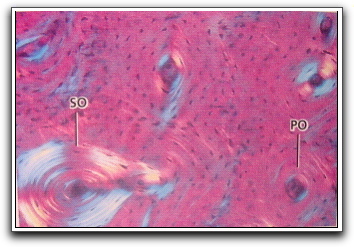
Los tipos de fibras que se pueden encontrar en el ligamento periodontal son: colágenas, reticulares, elásticas, oxitalánicas y de elaunina. Las fibras colágenas son las que representan el mayor componente fibrilar, principalmente de tipo I, III y V. A los grupos de fibras que se encuentran con una disposición ordenada, se les denomina fibras principales. La porción de las fibras principales que están incluidas en el hueso reciben el nombre de fibras de Sharpey, (Gráfico 23) y las insertadas en el cemento se denominan fibras perforantes, retenidas o incluidas,4,5,6,7 (Gráfico 24).
Estas fibras principales se dividen en 5 grupos, Grupo crestoalveolar u oblicuas ascendentes, se extienden desde la cresta alveolar hasta debajo de la unión cemento-esmalte, su función principal es evitar los movimientos de extrusión. Grupo horizontal o de transición, tienen una disposición en ángulo recto respecto al eje longitudinal del diente (desde el hueso hacia el cemento) y están localizadas inmediatamente por debajo de las fibras crestoalveolares. Su función principal es resistir las fuerzas laterales y horizontales. Estas fibras a diferencia de las otras se encuentran localizadas en dos áreas, a nivel cervical y apical.4,5,6,7
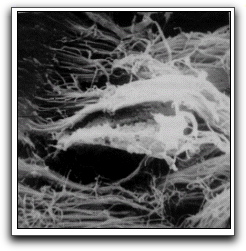 |
Gráfico 23. Zona de inserción de las fibras periodontales en el hueso. Nótese su disposición en haces. MEB. Tomado de Gómez y Campos. 1999. |
 |
|
|
Gráfico 24. Superficie del cemento. Se observan oquedades de inserción de las fibras perforantes. MEB, x 900. Tomado de Gómez y Campos. 1999. |
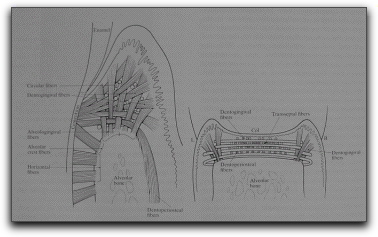
Grupo oblicuo descendente, son las fibras más numerosas y potentes, se disponen en posición descendente desde el hueso hacia el cemento, su finalidad es soportar las fuerzas masticatorias y de intrusión. Grupo apical, las fibras apicales irradian desde la zona del cemento que rodea el foramen apical, hacia el fondo del alvéolo, la misión de estas fibras es, evitar los movimientos de lateralidad y extrusión y amortiguar los de intrusión; no están presentes en dientes incompletamente formados. Grupo interradicular, solo está presente en los dientes multirradiculares, las fibras se ubican desde la cresta del tabique interradicular hacia el cemento en forma de abanico. Su función es evitar los movimientos de lateralidad y rotación,4,5,6,7 (Gráfico 25).
Las fibras de elaunina y oxitalán, son fibras elásticas inmaduras que ocupan el 3% del ligamento periodontal, siguen una dirección axial al diente, con un extremo incluido en el cemento o en el hueso, y el otro en la pared de un vaso sanguíneo o en el tejido conjuntivo. Son más abundantes en la zona apical y se cree que podrían tener la función de sostener los vasos del ligamento. Las fibras reticulares y elásticas son escasas y por lo general se hallan formando parte de las paredes de los vasos.4,5,6
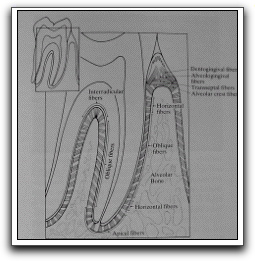 |
Gráfico 25. Fibras principales del periodonto funcional. El grupo de fibras del ligamento periodontal incluye a las crestoalveolares, horizontales, oblicuas, apicales e interradiculares. Tomado de Gutmann y Harrison. 1994. |
La sustancia fundamental del ligamento contiene ácido hialurónico, condroitín 4-sulfato, condroitín 6-sulfato, dermatán sulfato y heparán sulfato, el más abundante es el dermatán sulfato. También presenta un contenido elevado de agua (70%). Esta sustancia es indispensable para el mantenimiento y la función normal del tejido conjuntivo.5,6
Características anatómicas e histológicas del hueso alveolar: La apófisis alveolar o proceso alveolar, puede ser definida como aquella parte de los maxilares, superior e inferior, que forma y sostiene los alvéolos de los dientes.4,6 Es un tejido conjuntivo especializado cuya matriz extracelular está calcificada e incluye las células que lo secretan.9 Junto con el cemento y el ligamento periodontal, el hueso alveolar tiene como función principal distribuir y absorber las fuerzas generadas, por ejemplo, por la masticación y otros contactos dentarios.4
El hueso alveolar tiene dos componentes: el hueso alveolar propio y la apófisis alveolar. El hueso alveolar propio se continúa con la apófisis o proceso alveolar y forma la fina lámina ósea que está situada junto al ligamento periodontal.4
Radiográficamente se pueden distinguir dos tipos de hueso alveolar, la porción que cubre el alvéolo, también llamada hueso cortical y a veces denominada como lámina dura; y la porción de la apófisis alveolar que, radiográficamente, tiene un aspecto de red y se denomina hueso esponjoso.4
El hueso alveolar se forma durante el crecimiento fetal por osificación intramembranosa6 y es un tejido conjuntivo constituido por células y matriz extracelular. Contiene un 60% a 65% de sustancias minerales, 20 % de agua y 20% a 35% de componentes orgánicos.5,6,9 Alrededor del 90% de esta matriz orgánica está representada por fibras colágenas de tipo I.5,6,7,9 Entre los componentes minerales, el 80% corresponde a cristales de hidroxiapatita, 15% a carbonato de calcio y 5% a otras sales minerales.4,5,6,9
Las células que podemos encontrar en el hueso alveolar son: células osteoprogenitoras, osteoblastos, (Gráfico 26), osteocitos, (Gráfico 27), y osteoclastos,5,9 (Gráfico 26). Todas ellas fabrican, mantienen y remodelan al tejido óseo.5
Las unidades estructurales básicas del hueso cortical son los osteones (o sistemas de Havers), que son estructuras cilíndricas orientadas longitudinalmente, construidas alrededor de los conductos vasculares (o de Havers),4,9 (Gráfico 28). Cada conducto o sistema de Havers está recubierto por un capa de osteoblastos y células progenitoras que alojan a un haz neurovascular con su tejido conjuntivo. Los conductos de Havers contiguos están unidos entre sí por los conductos de Volkmann,9 (Gráfico 29). Los osteones secundarios se forman después del remodelado óseo y revelan un claro patrón de laminillas,4 (Gráfico 30).
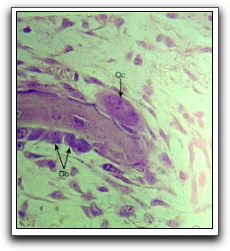 |
Gráfico 26. Fotomicrografía de la osificación intramembranosa (x540). Los osteoblastos (Ob) recubren la espícula ósea en donde secretan osteoide hacia el hueso. Se observan osteclastos (Oc) alojados en lagunas de Howship. Tomado de Gartner y Hiatt 2002. |
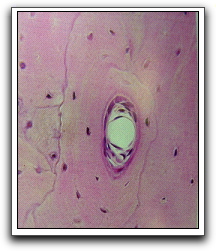 |
Gráfico 27. Fotomicrografía de hueso compacto descalcificado (x540). Pueden observarse osteocitos en lagunas. Véase asimismo la osteona y las líneas de cementación. Tomado de Gartner y Hiatt 2002. |
 |
Gráfico 28. Fotomicrografía de hueso esmerilado descalcificado (x270). Obsérvese el sistema de Havers que contiene el canal haversiano (C) y láminas concéntricas con lagunas y sus canalículos. (flechas). Tomado de Gartner y Hiatt 2002. |
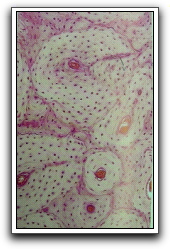 |
Gráfico 29. Fotomicrografía de hueso compacto descalcificado (x162). Se muestran varias osteonas con sus láminas concéntricas. También se identifica un conducto de Volkmann (V). Tomado de Gartner y Hiatt 2002. |
 |
|
|
|
Las unidades estructurales óseas, como los osteones y los paquetes, no son sólo estructurales sino además unidades metabólicas. La nutrición del hueso está asegurada por los vasos sanguíneos, éstos rodeados por laminillas óseas constituyen el centro de un osteón, en el cual, el conducto central (que contiene al vaso sanguíneo), recibe el nombre de conducto de Havers.4
Los alvéolos alojan a las raíces de los dientes y presentan dos tipos de paredes: las tablas alveolares libres (palatina, vestibular o lingual) y los tabiques alveolares interdentarios o interradiculares.5
En el maxilar superior las tablas vestibulares son más delgadas que las palatinas, en especial a nivel de los incisivos y caninos,4,5,8 (Gráfico 31), donde las paredes vestibulares están constituidas sólo por hueso compacto 5 ya que por lo general no existe hueso medular.8
En algunas ocasiones los incisivos laterales se encuentran en una posición muy palatina y por lo tanto presentan de 3 a 5mm de hueso medular, lo que hace difícil su abordaje y localización,8 (Gráfico 32).
 |
|
|
Gráfico 31. Corte transversal de la apófisis alveolar del maxilar superior a nivel de la porción radicular media de los dientes. Las paredes de los alvéolos están tapizadas por hueso compacto (flechas) y el área entre los alvéolos, incluida la pared ósea compacta, está ocupada por hueso esponjoso. Tomado de Lindhe. 2000. |
 |
 |
|
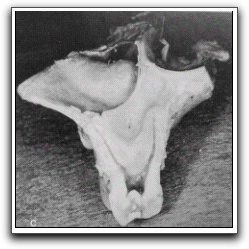
Gráfico 32. Incisivo lateral con la encía cubriendo el hueso, excepto la mitad apical labial. Obsérvese que la raíz ocupa una posición más palatina en el alvéolo. Por tanto, es mayor el grosor del hueso labial, menor el palatino y ha cambiado el eje longitudinal. Tomado de Arens, Adams y DeCastro 1984. |
Gráfico 33. Hueso bucal fino y palatino grueso. Las raíces distobucal y palatina están separadas del seno por una fina tabla cortical. Tomado de Arens, Adams y DeCastro 1984. |
En cuanto a los dientes posteriores la cortical vestibular es muy delgada (más delgada que la palatina), y el hueso medular es grueso a nivel de los premolares, de 3 a 4mm aproximadamente; en cambio en los molares puede estar ausente. En la zona palatina ambos son más gruesos que en vestibular,8 (Gráfico 33).
En el maxilar inferior las tablas vestibulares son bastante más delgadas que las linguales en la zona de incisivos y premolares,5,8 son frecuentes las dehiscencias cerca de la cresta alveolar en los incisivos y el hueso medular puede medir de 2 a 3mm de grosor, sobre todo a nivel de los caninos que puede llegar a medir hasta 5 mm; o si los incisivos se encuentran en una posición muy vestibular también presentarán mayor cantidad de hueso medular.8
En la región molar la cortical ósea vestibular tiene un grosor medio de 2 a 3mm, siendo la lingual un poco más gruesa, 8 en cambio el hueso alveolar es más grueso por la región vestibular que la lingual en los molares,5,8 (Gráficos 34, 35 y 36).
Radiográficamente el hueso compacto, que es la capa más periférica del hueso, se observa como una delgada lámina radiopaca, por esta razón la denominan lámina dura. Histológicamente éste es un tejido óseo laminar cuyas láminas corren paralelamente a la superficie alveolar. Esta lámina dura se encuentra atravesada por numerosos haces de fibras, llamadas fibras de Sharpey, que provienen del ligamento periodontal.4,5
El tejido óseo medular se encuentra muy desarrollado en los tabiques alveolares y se presenta también en algunas de las tablas, es un tejido compuesto por trabéculas, espículas y espacios medulares, por lo que presenta una imagen radiográfica de densidad variable. El tamaño y la forma de las trabéculas están determinados genéticamente, pero en parte también son resultado de la actividad de los procesos alveolares.5
Radiográficamente las trabéculas se pueden discriminar en dos tipos: trabéculas de tipo I, regulares, gruesas y horizontales, típicas del maxilar inferior; y las tipo II, finas, delicadas y dispuestas irregularmente, comunes en el maxilar superior.5
 |
|
|
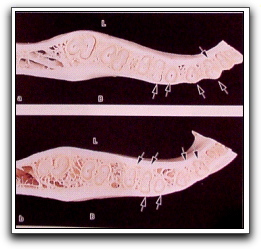
Gráfico 34. Cortes transversales de la apófisis alveolar mandibular, a niveles que corresponden a los tercios coronario (a) y al apical (b) de las raíces. El hueso que recubre las paredes de los alvéolos, se continúa con frecuencia con el hueso compacto cortical de lingual (L) y vestibular (B) de las apófisis alveolares (flechas). Tomado de Lindhe. 2000. |
 |
 |
|
Gráfico 35. El ápice está en el centro del proceso alveolar. El hueso cortical labial es ligeramente más fino que el lingual. Tomado de Arens, Adams y DeCastro 1984. |
Gráfico 36. Vista proximal de la raíz interna del primer molar que contiene un sistema canalicular tipo 2-1. El conducto mandibular se encuentra cerca del borde inferior de la mandíbula. Tomado de Arens, Adams y DeCastro 1984. |
Todas las superficies óseas están cubiertas por capas de tejido conjuntivo osteógeno diferenciado. La membrana que cubre la superficie externa del hueso se llama periostio, mientras que aquél que reviste las cavidades óseas internas se denomina endostio.6,9
La función principal del hueso alveolar es proporcionar los alvéolos para que el diente se aloje y se fije a ellos a través de las fibras periodontales, constituyendo la articulación alvéolodentaria que permite resistir las fuerzas de la masticación, además el hueso alveolar protege a los vasos y nervios del ligamento periodontal.4,5
Cicatrización de los Tejidos en la Cavidad Bucal. Generalidades
En el cuerpo humano existen tres grupos de células clasificadas de acuerdo a su capacidad proliferativa y su relación con el ciclo celular. El primer grupo de células son las llamadas células lábiles, las cuales recorren el ciclo celular desde una mitosis a la siguiente y proliferan durante toda la vida. Estas células se encuentran en el epitelio de la cavidad bucal, médula ósea y los tejidos hematopoyéticos, entre otros. Son células que poseen un gran potencial de regeneración.10
El segundo grupo de células son las células estables, las cuales muestran una actividad mitótica escasa, más sin embargo, pueden dividirse rápidamente ante ciertos estímulos. A este grupo pertenecen las células del tejido conjuntivo, fibroblastos, células endoteliales de los vasos, condrocitos, osteocitos, entre otras.10
Por último, existen las células permanentes, las cuales no pueden dividirse en la vida postnatal. A este grupo de células pertenecen la mayoría de las células nerviosas, las células del miocardio y las musculares esqueléticas.10 Debido a la naturaleza de los tejidos involucrados en un acto quirúrgico endodóntico, todos ellos tiene capacidad de regeneración a excepción de la dentina.11,12
Definición de cicatrización: Popularmente se le adjudica el término cicatrización a una herida cuando sana, pero este proceso es mucho más profundo y complejo de lo que parece e involucra una serie de acontecimientos biológicos; de hecho existen diferentes tipos de cicatrización y diferencias entre una reparación o una regeneración.13,14,15,16
El Diccionario terminológico de ciencias médicas define la cicatrización como el proceso de curación que da por resultado la formación de una cicatriz; puede efectuarse por primera o segunda intención.17 Mientras que el Diccionario ilustrado de Odontología explica la cicatrización como el proceso de curación por formación de tejido cicatricial y consiguiente exceso de colegenización con la producción de una cicatriz.18
Algunos autores también definen este proceso como reparación mediante tejido conjuntivo,14 o fibroplasia o fibrosis 10 y acotan que cuando existe una lesión tisular grave o persistente e inflamación con daño a las células parenquimatosas, conducen a una situación donde la reparación no se puede lograr por la simple regeneración del parénquima.14
Aunque una cicatriz se puede considerar funcionalmente imperfecta, es importante resaltar que ella cubre el defecto en el tejido y permite que el parénquima residual continúe funcionando.14
Harrison y Jurosky 19 definen la cicatrización como la respuesta de los tejidos vivos a cualquier injuria que cause interrupción de la continuidad y/o función de algún tejido, la cual involucra una serie de eventos biológicos complejos que pueden ocurrir simultáneamente o no. La cicatrización básicamente depende del tipo de tejido lesionado y la clase de herida realizada.
Para concluir se sabe que existen dos tipos de cicatrización, primera y segunda intención y tres componentes durante el proceso angiogénesis, fibrosis y remodelado,14,15 puntos que serán explicados más adelante.
Definición de reparación: En la literatura revisada uno de los autores que con más claridad ha definido estos términos ha sido Garrett,13 él define reparación como la cicatrización de una herida por un tejido que no es completamente restaurado en arquitectura o función.
Según el Diccionario ilustrado de odontología,18 es la restauración física o mecánica de tejidos dañados o enfermos mediante el crecimiento de nuevas células sanas o por aposición quirúrgica.
Para Harrison 20 la reparación de los tejidos se obtiene cuando los bordes de la herida no se encuentran próximos y se forma una gran cantidad de tejido de granulación que funciona como puente del hiato debiéndose esto al mecanismo de cicatrización por segunda intención.
La reparación de un tejido por lo general se considera como una fase de la reacción inflamatoria,21,16 por lo tanto, se inicia al principio de la inflamación e implica dos procesos separados, la regeneración del tejido lesionado por células parenquimatosas del mismo tipo y la sustitución por tejido conjuntivo que producen una cicatriz permanente.14
Los dos principales agentes que interviene en este proceso son los macrófagos, quienes limpian el tejido y los fibroblastos, quienes remiendan el daño.21
Ambas células actúan en la periferia del foco inflamatorio y un buen ejemplo de esto es lo que ocurre en la pared de un absceso, la cual tiene un espesor aproximado de 2 mm; en el interior de la superficie, los polimorfonucleares continúan actuando mientras que a 1 o 2 mm de distancia se encuentran los macrófagos que remueven los restos de tejido y los fibroblastos que tapizan las paredes del defecto, comenzando la formación de la cicatriz.21
En conclusión, la reparación es el mecanismo mediante el cual un tejido lesionado o perdido, de cualquier tipo, es sustituido inicialmente por una masa de tejido conjuntivo fibroso.21
En periodoncia cuando la cicatrización es por reparación sólo se restituye la continuidad de la encía marginal enferma y el surco gingival se reestablece en la base del saco periodontal preexistente.22
Definición de reinserción: La reinserción es la reparación del tejido sobre una superficie radicular que nunca ha sido expuesta a enfermedad periodontal. Ella se puede lograr después de realizar una incisión intrasulcular o desgarro traumático de los tejidos gingivales.13,22
Definición de nueva inserción: La nueva inserción se describe como el establecimiento de nuevas fibras del ligamento periodontal insertadas en un nuevo cemento radicular y epitelio gingival, sobre una superficie radicular que previamente estuvo privada de su aparato de inserción original.13,22
Definición de regeneración: En el Diccionario terminológico de ciencias médicas 17 también se encuentra el concepto de regeneración, donde se define como la reproducción de una parte, tejido u órgano desaparecido.
También se ha descrito como el crecimiento y diferenciación de nuevas células y sustancia intercelular para formar nuevos tejidos o partes. En el tejido oral consiste en fibroplasia, proliferación endotelial y aposición de sustancia fundamental intersticial, colágeno y maduración del tejido conjuntivo. Se produce por crecimiento del mismo tipo de tejido que el destruido o a partir de su precursor. 18
Según Harrison 20 se produce regeneración de los tejidos cuando éstos han sido restaurados completamente hasta obtener un patrón anatómico y funcional normal e igual a los que previamente existían, 20,23 señalando que éste es el resultado del mecanismo de cicatrización por primera intención. 20
Robbins et al.10 refieren que es la sustitución de las células lesionadas o perdidas por otras de la misma clase, a veces sin que queden huellas residuales de la lesión anterior. Pero no todos los tejidos tienen ésta capacidad y cuando la regeneración no es posible, se produce una reparación.21
Así mismo, Garrett1 3 también describe la regeneración como la reproducción o reconstitución de una parte dañada o perdida por medio de un proceso biológico por el cual la arquitectura y función de los tejidos perdidos es completamente restaurada. En el caso de la regeneración periodontal, todos los tejidos que soportan al diente hueso alveolar, ligamento periodontal y cemento, recuperan su finalidad. 13,23
Clasificación y descripción de los tipos de cicatrización
Los clínicos utilizan los términos primera intención y segunda intención, para referirse a las dos formas básicas de cicatrización de las heridas.10,11,14-16 Sin embargo, el que una herida cure por primera o segunda intención depende de si los bordes son reposicionados y no del propio proceso de la curación. 10
Cicatrización por primera intención: La cicatrización por primera intención ocurre cuando los bordes de una herida han sido reposicionados por cualquier medio, hallándose entre estos bordes un pequeño coágulo.11,14,16
En estos casos los bordes de la herida se encuentran anatómicamente en el mismo lugar que antes de producirse el daño al tejido. La reparación ocurrirá más rápidamente y con menor riesgo de infección, con una mínima formación de cicatriz debido a que el tejido prácticamente no percibió ninguna injuria.15
El resultado final de este tipo de cicatrización es la regeneración, por lo tanto, el tejido lesionado es restaurado en función y anatomía a como era originalmente.11
Durante el primer día en el proceso de cicatrización por primera intención, se observan polimorfonucleares neutrófilos en el borde de la incisión que se desplazan hacia el coágulo de fibrina. Las células basales en el borde de la herida comienzan a mostrar mayor actividad mitótica y a las 24 a 48 horas después las células epiteliales de ambos bordes se desplazan y proliferan produciendo una capa de epitelio, delgada pero continua.14
Al segundo y tercer día los polimorfonucleares neutrófilos han sido sustituidos sobre todo por macrófagos y la incisión es invadida por tejido de granulación. Para este momento ya son evidentes las fibras de colágeno en los bordes de la incisión, pero se encuentran en una disposición vertical que no une los bordes. Las células epiteliales continúan proliferando haciendo la capa más gruesa.14
Entre el cuarto y quinto día la neovascularización alcanza su máximo a medida que la incisión se rellena con tejido de granulación. En este punto, las fibras de colágeno son más abundantes y comienzan a unir los bordes de la herida. Mientras transcurre la segunda semana, el colágeno continúa acumulándose y los fibroblastos siguen proliferando; pero el edema, infiltrado leucocitario y la vascularización incrementada, disminuyen considerablemente.14
Ya para el primer mes la cicatriz presenta un tejido conjuntivo desprovisto de células inflamatorias y con el tiempo la herida aumenta su resistencia a la tensión.14
Cicatrización por segunda intención: Cuando los bordes de una herida se encuentran separados y existe un coágulo grueso entre ellos, se requiere mayor formación de tejido de granulación. El resultado final de este proceso es la reparación debido a que el tejido no es restaurado con un patrón y función normal.11,16
Si la pérdida del tejido es muy extensa, el proceso de reparación es más complejo, la sola regeneración de las células del parénquima no pueden restablecer la estructura original. Como consecuencia se produce un extenso crecimiento hacia adentro del tejido de granulación a partir del borde de la herida, seguido con el tiempo por acumulación de matriz extracelular y de cicatriz. Esta forma de cicatrización se conoce como unión secundaria o cicatrización por segunda intención.14
La cicatrización por segunda intención se diferencia de la cicatrización por primera intención en varios aspectos: los grandes defectos en el tejido tienen un mayor volumen de residuos necrosados, exudado y fibrina que deben ser eliminados. Como consecuencia la reacción inflamatoria es más intensa.14
Se forma una cantidad mayor de tejido de granulación para llenar las brechas de la estructura estromal y por lo general se produce mayor masa de tejido cicatricial; en la cicatrización por segunda intención, se observa el fenómeno de contracción de la herida (entre un 5 y 10%), se cree que esto es debido a la presencia de miofibroblastos.14 Por lo tanto, este tipo de cicatrización será más lenta y producirá mayor cicatriz.15
Descripción de las etapas del proceso de cicatrización
La cicatrización de una herida quirúrgica comienza inmediatamente después de realizar la sutura.21 Por lo general se toma como referencia a la curación de las heridas de la piel para ilustrar los principios generales de la curación de las heridas que son aplicables a todos los tejidos.10
El corte que realiza la hoja de bisturí causa un daño a millones de células y vasos sanguíneos, se derrama sangre y se forma un coágulo entre los bordes de la herida.21
La cicatrización de una herida implica procesos complejos como: inducción de una respuesta inflamatoria aguda por la liberación de aminas y otros mediadores de la inflamación; regeneración de las células parenquimatosas; migración y proliferación de las células parenquimatosas y de tejido conjuntivo; síntesis de las proteínas de la matriz extracelular; remodelación de los elementos parenquimatosos para restablecer la función del tejido y finalmente remodelación del tejido conjuntivo para proporcionar resistencia a la herida.14,21
Una lesión grave a los tejidos o inflamación con daño a las células parenquimatosas y estroma, conducen a una situación en la cual la reparación no se puede lograr por la simple regeneración del parénquima, por esto, estas células no regeneradas son reemplazadas antes de las 24 horas por fibroblastos proliferantes y células endoteliales vasculares.14
Aproximadamente entre 3 y 5 días después, se establece un tejido de granulación indicador de cicatrización14 y para la primera semana la herida se encuentra rica en células, especialmente macrófagos y fibroblastos; pero al transcurrir los días esta población celular disminuye y se incrementa el material intercelular.21
Finalmente, el tejido de granulación se acumula y con el tiempo produce una fibrosis o cicatrización. Durante este proceso existen tres etapas fundamentales, la etapa inflamatoria; la etapa fibroplástica y la etapa de remodelado.14,15
Etapa inflamatoria: También es conocida como el proceso de angiogénesis o neovascularización.14 La etapa inflamatoria presenta dos formas bien diferenciadas, aguda y crónica. La inflamación aguda es de evolución relativamente breve y sus características principales son el exudado de líquido y proteínas plasmáticas, lo que origina el edema y la migración de leucocitos, predominantemente neutrófilos.24
La inflamación crónica tiene una duración mayor y se caracteriza por la presencia de linfocitos y macrófagos, la proliferación de vasos sanguíneos, fibrosis y necrosis tisular. En la inflamación crónica se pueden observar simultáneamente signos de inflamación activa, de destrucción tisular y de intentos de curación.24
La respuesta inflamatoria está muy relacionada con el proceso de reparación. La inflamación es útil para destruir, atenuar o mantener localizado al agente patógeno y al mismo tiempo inicia una cadena de acontecimientos que dentro de lo posible, curan y reconstruyen el tejido lesionado.24
La inflamación es fundamentalmente una respuesta de carácter protector cuyo objetivo final es liberar al organismo de la causa inicial de la lesión celular. Si no existiera el proceso de inflamación, las heridas no se curarían nunca; sin embargo, los procesos de inflamación y reparación pueden ser perjudiciales.24
La inflamación comienza cuando el tejido es dañado y se caracteriza por presentar dos fases: la vascular y la celular.15 Las respuestas vascular y celular de las formas aguda y crónica de la inflamación están mediadas por factores quimiotácticos procedentes del plasma o de las células que son activados por el propio estímulo inflamatorio.24
El evento vascular se inicia con la vasoconstricción de los vasos rotos, el cual disminuye el flujo sanguíneo en el lugar de la herida y promueve la coagulación; en cuestión de minutos se elabora histamina y prostaglandinas E1 y E2 que causan vasodilatación y permiten la salida de plasma y leucocitos.15,24
Posteriormente, el acúmulo de líquido extravascular rico en proteínas, la acumulación de fibrina proveniente del plasma y la obstrucción linfática, da lugar a la formación del edema. Inmediatamente después de este evento, se manifiestan los signos cardinales de la inflamación (rubor, dolor, calor y pérdida de la función).15,24
La fase celular de la inflamación es desencadenada por la activación del sistema de complemento en el tejido traumatizado, particularmente C3a y C5a que actúan como factores quimiotácticos que estimulan la salida de los neutrófilos; algunos neutrófilos una vez que entran en contacto con algún cuerpo extraño (bacterias o tejido necrótico), se degranulan y liberan sus lisosomas; mientras que otros fagocitan al agente lesivo. Al mismo tiempo, se acumulan macrófagos y linfocitos en el sitio de la lesión.15,24
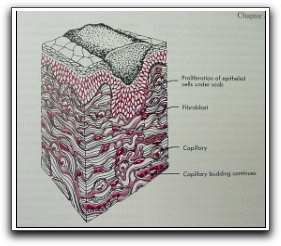
Simultáneamente al proceso vascular inicial y la fase celular, comienza la formación de vasos nuevos en el lugar donde se realiza el proceso de reparación. Estos vasos nuevos permiten la salida de líquido a través de sus uniones interendoteliales, que aún están incompletamente formadas, lo que hace que el tejido de granulación luzca edematoso inclusive después de que el proceso inflamatorio a cesado.14 Pocos días después, se reestablece la circulación a través de los márgenes de la herida,21 (Gráfico 37).
Durante la etapa inflamatoria aguda se liberan una serie de mediadores químicos que modulan la respuesta vascular y celular. Los mediadores que principalmente están involucrados son: la histamina, las anafilatoxinas (C3a y C5a), las quininas, los leucotrienos C, D y E, el PAF y la sustancia P. También se liberan prostaglandinas las cuales desempeñan un papel importante en la vasodilatación, el dolor y la fiebre, así como en la intensificación del edema.24
 |
|
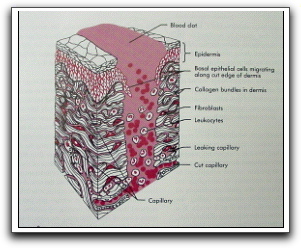
|
Gráfico 37. Etapa inflamatoria de la reparación de las heridas. La herida se rellena con un coágulo de sangre, células inflamatorias y plasma. El epitelio adyacente comienza a migrar hacia la herida y las células mesenquimatosas indiferenciadas comienzan a transformarse en fibroblastos. Tomado de Peterson et al. 1998. |
Etapa fibroplástica: En esta etapa la malla de fibrina proveniente de la coagulación de la sangre, permite que los fibroblastos comiencen a depositar tropocolágeno aproximadamente tres o cuatro días después del daño. Pero los fibroblastos también secretan fibronectina, la cual ayuda a estabilizar a la fibrina.15
La fibrosis o fibroplasia se produce sobre los vasos nuevos en el tejido de granulación y sobre la matriz extracelular laxa que se desarrolla inicialmente en el sitio de la reparación. El reclutamiento y estimulación de los fibroblastos es mediado por diversos factores de crecimiento.14
Los factores de crecimiento son moléculas polipéptidas liberadas por las células en el área inflamada, las cuales regulan los eventos en la cicatrización de las heridas.10,23,25
Algunos de los fenómenos celulares que estimulan son: la proliferación celular, quimiotaxia, diferenciación y producción de proteínas de la matriz extracelular, entre otros. Se consideran como hormonas que no se descargan al torrente sanguíneo y tienen sólo acción local.10,23,25 Existen varios factores de crecimiento involucrados en la curación de las heridas,10 (Tablas I y II).
Dentro de la etapa fibroplástica los macrófagos juegan un papel muy importante ya que se encargan de la eliminación de los residuos extracelulares, polimorfonucleares muertos, fibrina y cuerpos extraños en el sitio de la lesión; además promueven la proliferación y migración de los fibroblastos.14,21,24

Tabla I. Los factores de crecimiento en la curación de las heridas. Tomado de Robbins et al. 2000.

Tabla II. Nomenclatura de los factores de crecimiento en la curación de las heridas. Tomado de Robbins et al. 2000.
A medida que el proceso de cicatrización avanza, el número de fibroblastos y vasos neoformados disminuye; y el colágeno participa de forma decisiva en el desarrollo de la resistencia de la herida.14,21 Es por esto que como regla general se acepta que en las lesiones recientes existen muchas células y en las lesiones menos recientes existen más fibras colágenas.21
La síntesis de colágeno se inicia desde que comienza el proceso de cicatrización (3 a 5 días) y continúa durante varias semanas dependiendo del tamaño de la lesión. Finalmente el tejido de granulación evoluciona para formar una cicatriz compuesta de fibroblastos, colágeno denso, fragmentos de tejido elástico y otros componentes de la matriz extracelular,14 (Gráficos 38 y 39).
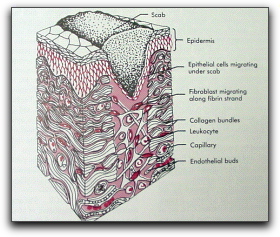 |
Gráfico 38. Fase migratoria de la etapa fibroplástica de la reparación de las heridas. La migración epitelial continúa y los leucocitos eliminan los materiales necróticos y extraños, comienzan a crecer los capilares y los fibroblastos migran hacia la herida a lo largo de la malla de fibrina. Tomado de Peterson et al 1998 |
|
|
Gráfico 39. Fase proliferativa de la etapa fibroplástica de la reparación de las heridas. Se incrementa la proliferación epitelial y los fibroblastos colocan al azar las fibras colagenas y los capilares comienzan a establecer contacto con sus contrapartes del otro lado de la herida. Tomado de Peterson et al. 1998. |
Etapa de remodelado: El resultado final de los procesos de síntesis y degradación, es el remodelado del tejido conjuntivo que es una característica importante tanto de la inflamación crónica como de la reparación de las heridas.10 Esta etapa puede continuar indefinidamente en el tiempo y también es conocida con el nombre de maduración de la herida.15
El remodelado de la cicatriz requiere de la descomposición del colágeno el cual ayuda al debridamiento de los sitios lesionados para lograr la reparación del defecto.14 Es por esto que muchas fibras son destruidas y son reemplazadas por nuevas mejor orientadas.15
Durante esta etapa una serie de enzimas producidas por los fibroblastos, macrófagos, neutrófilos y algunas células epiteliales, son liberadas de forma controlada e inactiva, posteriormente son activadas por la acción de ciertas sustancias o proteasas que se encuentran en el sitio de la lesión.14
El proceso culmina con la contracción de la herida que aproxima aún más los bordes de la lesión, lo que trae como consecuencia disminución de su tamaño y reducción en su elasticidad.15 Cabe destacar que este es el proceso de cicatrización que ocurre en ausencia de infección, ya que el desarrollo de una infección prolonga la fase inflamatoria y retrasa la cicatrización,21 (Gráfico 40).
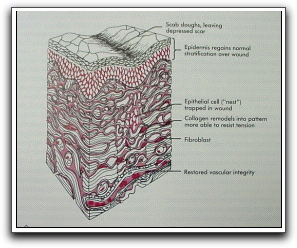 |
Gráfico 40. Etapa de remodelado de la reparación de las heridas. Es restaurada la estratificación epitelial, el colágeno es remodelado a un patrón más eficiente y organizado. Tomado de Peterson et al. 1998. |
Robbins et al.10 refiere que los procesos de la inflamación y reparación ponen de relieve la considerable capacidad del cuerpo humano para recuperarse por sí mismo, sobrepasando la eficacia de cualquier ingenio construido por los seres humanos.
Proceso de Cicatrización de los tejidos blandos, periapicales y radiculares.
Las bacterias son la causa principal y más común de inflamación pulpar y periapical.26-28 De hecho la relación entre la inflamación periapical y la infección bacteriana 27,28 quedó muy bien establecida en el estudio de Kakehashi en 1965.29
Las bacterias y sus componentes pueden alcanzar al tejido periodontal a través del orificio apical o de los conductos accesorios, lo que trae como consecuencia el establecimiento de una periodontitis.26,27 La severidad de la inflamación periapical se ha relacionado directamente con los microorganismos dentro del sistema de conductos radiculares y a su exposición prolongada.27,30
El tejido periapical reacciona ante las bacterias como cualquier tejido conjuntivo del organismo y por consiguiente intervienen los mismos mediadores o sustancias químicas de la inflamación antes descritos.26
La presencia de una periodontitis apical es un prerrequisito para realizar una cirugía endodóntica. Por lo tanto, una imagen radiolúcida persistente después de ejecutar un adecuado retratamiento endodóntico, podría ser una indicación para un tratamiento quirúrgico.31
La mayoría de las lesiones periapicales cicatrizan de forma irregular después de un tratamiento endodóntico.32 La cirugía endodóntica se ejecuta para erradicar los irritantes provenientes del sistema de conductos radiculares y eliminar las causas potenciales de una inflamación periapical persistente 32-34 y de esta forma permitir la reparación de los tejidos periapicales.34
La eliminación de las bacterias y sus componentes antigénicos del interior de los conductos radiculares, es el factor determinante para el predominio de los mediadores que favorecen la reparación y la disminución de los que propagan la inflamación. 26
Gutmann 35 refiere que cuando existe una gran posibilidad de fracasar con un tratamiento endodóntico no quirúrgico, o si el fracaso es el resultado de un tratamiento o retratamiento endodóntico y es imposible obtener un mejor resultado con la terapia convencional, está indicada la cirugía endodóntica. También existe una tercera indicación, cuando se requiere tomar una biopsia en o cerca del ápice radicular.27,35
Harrison 11 refiere que es una equivocación pensar que la cicatrización de los tejidos blandos y óseos después de una cirugía periapical es la misma que ocurre después de un procedimiento de cirugía periodontal mucoperióstico. De hecho, la cirugía periapical difiere marcadamente de otros procedimientos quirúrgicos odontológicos.
La cirugía periodontal por lo general altera intencionalmente y remueve las enfermedades de los tejidos blandos y duros, dependiendo del tipo de procedimiento y colgajo que se realice la cicatrización será por primera o segunda intención. Mientras en la cirugía periapical, casi siempre se manipulan hueso de soporte y tejidos blandos sanos, por lo tanto la cicatrización de los tejidos mucoperiósticos, en la mayoría de los casos será por primera intención.11
Es importante recalcar que el proceso de cicatrización varía dependiendo del tipo de tejido lesionado y el tipo de daño que el tejido recibe. Por lo general un mismo tipo de tejido responde de manera similar a la cicatrización.11
Cicatrización mucoperióstica: Aunque por ser tejidos del mismo tipo, deberían cicatrizar de manera similar; los tejidos blandos bucales lo hacen de forma más rápida que la piel. El tejido mucoperióstico está compuesto por la encía adherida, marginal e interdental y por debajo de ella se encuentra la mucosa alveolar y el periostio.11
Se ha reportado que a las 3 semanas existe una cicatrización completa y periodonto de protección sano después de realizar un colgajo mucoperióstico, si los tejidos marginales han sido reposicionados adecuadamente.36
Además, sí los tejidos blandos y óseos no se encuentran enfermos y se realiza una adecuada técnica quirúrgica y cuidado postoperatorio, se puede devolver la función y anatomía normal. Pero por el contrario, si hay presencia de gingivitis o periodontitis, es de esperarse alteraciones postquirúrgicas en el nivel de reinserción del periodonto y cresta ósea.11
Cicatrización de la herida incisional: La incisión define el perímetro del colgajo y se efectúa con una hoja de bisturí.11,19 Cuando se realiza se desencadenan una serie de mecanismos complejos y diversos.11
Los resultados del estudio de Harrison y Jurosky 19 indicaron que la cicatrización de los tejidos blandos era marcadamente rápida y similar, tanto en los colgajos triangulares como los rectangulares submarginales, aunque en los colgajos rectangulares era menos predecible.
También indicaron que la pérdida de inserción del tejido blando después de realizar una incisión intrasulcular en una cirugía perirradicular no era inevitable y se podía prevenir si se mantenía la vitalidad de los tejidos de inserción. Esto se pudo lograr evitando realizar el legrado de la supracresta de la superficie radicular y previniendo la deshidratación de estos tejidos con frecuente irrigación.19
El proceso de cicatrización de la herida incisional se puede describir en cuatro fases que no ocurren de forma separada: coagulación e inflamación; cicatrización epitelial; cicatrización del tejido conjuntivo y maduración y remodelado.11
Coagulación e inflamación: El primer requisito para la cicatrización es el efecto de hemostasia. Cuando un vaso es dañado se liberan mediadores químicos que causan una contracción vascular inicial transitoria y seguidamente ocurre una vasodilatación sostenida que conlleva al aumento de la permeabilidad vascular, mientras tanto en los vasos lesionados se forma un tapón plaquetario.11,15,24
Simultáneamente los mecanismos de coagulación intrínsecos y extrínsecos se disparan y se forma un coágulo, el cual actúa como un sellado viscoso entre la cavidad bucal y el tejido mucoperióstico lesionado y a su vez mantiene levemente unidos los bordes de la herida. Este fenómeno ocurre minutos después de la manipulación quirúrgica de los tejidos.11
Evidentemente, cuando un tejido es lesionado se produce una respuesta inflamatoria que involucra una reacción celular vascular y humoral. La cicatrización va a depender del proceso inflamatorio que proveerá un ambiente favorable.11,15,24
Inicialmente se produce una respuesta inflamatoria inmediata mediada por la liberación de mediadores químicos. La mayor cantidad de células activadas observadas en esta fase son los polimorfonucleares neutrófilos, que se encargan de fagocitar microorganismos, restos de tejido y liberar lisozimas.11,15,24
Los neutrófilos no pueden replicarse y tienen una vida promedio extravascular de 48 horas aproximadas. Después de transcurridas 24 a 48 horas la actividad de los neutrófilos disminuye y su número desciende rápidamente. El papel que juegan estas células en la cicatrización es muy importante ya que ellas destruyen rápidamente los microorganismos antes de que se establezca una infección.11,19
Alrededor de 6 a 12 horas después de lesionarse el tejido, aparecen los monocitos que al pasar hacia los tejidos reciben el nombre de macrófagos o fagocitos mononucleares, que son altamente móviles, con capacidad de replicación y mayor vida (meses o años).11,19
Seguidamente a este mecanismo de defensa primario, el sistema inmune se dispara y se produce una respuesta inmune humoral y una respuesta inmune mediada por células. La respuesta humoral consiste en la activación de los linfocitos B, los cuales secretan anticuerpos en contra de los antígenos. En cambio los linfocitos T activados, son los responsables de la respuesta inmune mediada por células la cual se encarga de atacar y neutralizar antígenos específicos.11
Durante las primeras 48 horas se produce la síntesis de fibroblastos y colágeno, esenciales para la angiogénesis.11,14,15
Regeneración epitelial: La cicatrización del tejido conjuntivo depende de la regeneración epitelial y el primer paso para que esto ocurra es la epitelialización en la superficie del coágulo de fibrina. Pocas horas después de producirse la lesión, las células de la capa basal y suprabasal comienzan a multiplicarse y cruzan el coágulo de fibrina. La migración culmina cuando la célula epitelial entra en contacto con otra del mismo tipo (inhibición de crecimiento por contacto); seguidamente se establece un sellado o puente epitelial y finalmente por el proceso de maduración las células epiteliales se diferencian y forman una capa de epitelio escamoso estratificado.11
La formación de esta barrera epitelial tiene dos funciones: prevenir el ingreso de irritantes bucales e inhibir el egreso de fluidos desde los tejidos. Mientras el coágulo de fibrina proporciona una ligera unión, la barrera epitelial provee resistencia al desalojo o separación de los bordes de la herida.11
Por lo tanto, la clave del éxito para una cicatrización rápida es la pronta epitelialización de la superficie de la herida incisional. Por lo general se acepta que este proceso ocurre entre las primeras 21 horas a 72 horas.11
Harrison y Jurosky 19 refieren que en la incisión vertical la formación del epitelio ocurre durante las primeras 48 a 72 horas, mientras que en la incisión intrasulcular la formación del epitelio se observa después de las 96 horas. La mucosa suele cicatrizar por primera intención debido a que los bordes de la herida son reposicionados uno frente al otro.37,38
Durante el levantamiento de un colgajo mucoperióstico intrasulcular se destruye la unión epitelial y parte del tejido conjuntivo, lo que trae como consecuencia retardo del proceso de cicatrización y debilitamiento del aparato de inserción. Es esta una de las razones de porque el cirujano endodóntico debe evitar este tipo de incisiones.11
En cuanto a la sutura quirúrgica, su función es mantener unidos los bordes de la herida, pero a su vez, ésta actúa como una barrera que causa variaciones en el proceso de cicatrización epitelial. Es por esto que se recomienda la remoción de la sutura lo más pronto posible.11
Cicatrización del tejido conjuntivo: Cuando la cicatrización ocurre por primera intención, el tejido conjuntivo comienza a cicatrizar cuando se forma el puente de epitelio y progresa rápidamente después de la maduración y formación de la barrera epitelial.11,19 La síntesis de colágeno es evidente dentro de las 24 horas después de la formación de la barrera epitelial.19
Las principales células involucradas en este proceso son los fibroblastos, los cuales sintetizan sustancias y elementos esenciales para la regeneración o reparación de las heridas. Ellos son atraídos hacia el lugar de la lesión por los factores quimiotácticos celulares y humorales del hospedero. Los macrófagos también juegan un papel importante en esta fase.11,14,15,24
El primer colágeno que se forma aparece como una fina red de fibras de colágeno tipo III (reticular), el cual es producido por las células ectomesenquimatosas indiferenciadas y los fibroblastos. Posteriormente estas mismas células comienzan a formar colágeno tipo I. La síntesis y degradación del colágeno es continua.11
Cuando el proceso de cicatrización de la herida progresa, la cantidad de macrófagos disminuye y los fibroblastos se convierten en las células predominantes, es entonces cuando se habla de tejido de granulación, el cual está pobremente organizado debido a que existe gran cantidad de sustancia fundamental y colágeno débil, pero gradualmente el colágeno madura. En este momento el coágulo de fibrina ha sido reemplazado por tejido conjuntivo (de granulación) y por lo tanto se considera que el coágulo se ha organizado completamente.11
Maduración y remodelado: Si la cicatrización es por primera intención, una vez que se ha formado suficiente colágeno, el número de fibroblastos decrece y simultáneamente también hay reducción de la vasculatura. La reducción en el número de fibroblastos marca el final de la etapa de cicatrización del tejido conjuntivo y da comienzo a la fase de maduración y remodelado.11
El tejido de granulación se sustituye por tejido conjuntivo joven y la orientación inicialmente de las fibras colágenas paralelas a la línea de incisión es ahora al azar. La maduración y remodelado de una herida, en condiciones ideales, comienza a los cinco a siete días después de realizada la incisión.11
La maduración y remodelado involucra simultáneamente la degradación y agregación del colágeno, lo que trae como consecuencia cambios en la arquitectura y densidad de las fibras, pareciéndose a la lámina propia normal.11,14,15
Una vez que la arquitectura y densidad se parece a la normal, la población de fibroblastos disminuye a los mismos niveles que el tejido circundante. El tiempo en que comienza y termina esta fase todavía es desconocido.11
Cuando la cicatrización es por segunda intención, el volumen de colágeno producido es mayor debido a la presencia de un gran hiato entre los bordes de la herida. Esto es bastante común en las incisiones semilunares debido a que a veces es muy difícil o imposible mantener los bordes unidos,11 (Gráficos 41, 42 y 43).
Cicatrización de la herida diseccional: La herida diseccional es el resultado de la elevación del colgajo mucoperióstico de la cortical ósea, la cual se realiza con un elevador de periostio romo para separar los tejidos blandos y proporcionar el acceso quirúrgico a los tejidos perirradiculares.39
 b) b) |
|
|
Gráfico 41. Diagrama representativo de la cicatrización de la herida incisional en los tejidos mucoperiósticos de la cavidad oral. (a) La herida incisional resulta en la discontinuidad del tejido vital (zona de la herida) rodeada por los tejidos adyacentes lesionados (bordes de la herida); (b) Formación del coágulo de fibrina en la zona de la herida, el cual conecta los bordes de la herida formando la vía para que las células reparadoras e inflamatorias migren. Tomado de Gutmann y Harrison. 1994. |
|
 d) d) |
|
|
Gráfico 42. Diagrama representativo de la cicatrización de la herida incisional en los tejidos mucoperiósticos de la cavidad oral. (c) Formación del sellado epitelial por migración de células epiteliales a través de la herida entre el coágulo de fibrina y la superficie del coágulo; (d) Proliferación y maduración de las células resultando en la formación de una barrera epitelial, síntesis de sustancia fundamental y colágeno, formación de tejido de granulación en la zona de la herida. Tomado de Gutmann y Harrison. 1994. |
|
 |
|
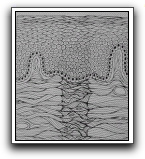
|
Gráfico 43. Diagrama representativo de la cicatrización de la herida incisional en los tejidos mucoperiósticos de la cavidad oral. (e) Continuación de la cicatrización con marcada remodelación y maduración de los tejidos, restauración de la arquitectura normal. Tomado de Gutmann y Harrison. 1994. |
Al reflejar un colgajo mucoperióstico usualmente se dejan restos de periostio sobre la superficie de la cortical ósea. Este remanente avascular evidencia destrucción celular y degeneración del colágeno en los primeros días, pero sobre todo durante las primeras 24 horas postoperatorias.11,39 Se ha sugerido que la degeneración del colágeno juega un papel importante en la reinserción rápida de los tejidos a la cortical ósea.39
La cicatrización de la herida diseccional ocurre prácticamente de la misma forma que la herida incisional, pero a menor velocidad;11,39 excepto por dos aspectos, el primero es que el epitelio no está involucrado en el proceso11 y segundo, ambos bordes no contribuyen de la misma forma en la fase de cicatrización del tejido conjuntivo.11,39 Esto es debido a que se produce un borde de la herida mucoperióstico y del lado opuesto, otro borde que se corresponde con la cortical ósea denudada.11
En el lugar de la herida se forma un coágulo de fibrina que debe organizarse en tejido de granulación, pero este tejido deriva de un solo borde de la herida, el mucoperióstico, ya que el borde de la cortical denudada contribuye poco o nada al respecto.11
Harrison y Jurosky 39 evidenciaron en su estudio realizado en monos, que para el cuarto día, el coágulo de fibrina ya ha sido reemplazado por tejido de granulación y a los catorce días se pudo observar la formación de tejido conjuntivo fibroso.
Durante los primeros 8 a 10 días, no se observa actividad osteoblástica u osteoclástica sobre la superficie perióstica de la tabla cortical. Para los 14 días, la actividad osteoclástica es limitada.11
A medida que la cicatrización avanza, las fibras colágenas de los restos de periostio son sustituidas por tejido de granulación organizado. A los 14 días, este tejido de granulación ha madurado y se puede observar un periostio joven y altamente vascular, el cual difiere del periostio normal. Posteriormente, a los 28 días, el periostio adquiere una apariencia microanatómica más normal y las áreas de resorción cortical muestran una evidencia temprana de reparación debido a la actividad osteoblástica.11
En cuanto a la cresta ósea, la actividad osteoclástica ocurre solo en la superficie del ligamento periodontal, de 3 a 4 días después de levantar el colgajo mucoperióstico. Esta actividad es mínima y a los 14 días se inicia la actividad osteoblástica para reparar el hueso reabsorbido. Para el día 28, la cresta ósea se observa microscópicamente normal.11,39
Harrison y Jurosky 39 no encontraron diferencias durante la cicatrización de la herida diseccional al realizar colgajos triangulares o rectangulares submarginales. También refieren que no observaron pérdida de la altura de la cresta ósea y aunque observaron actividad osteoclástica a ese nivel, en ambos colgajos hubo reparación osteoblástica.
Cicatrización periapical y radicular: Durante la cirugía endodóntica es necesaria la remoción de hueso para exponer el tercio apical de la raíz, por lo tanto se crea una herida excisional, la cual difiere de la herida incisional y diseccional,11 (Tabla III).

Tabla III. Esquema diferencial entre la herida incisional, diseccional y excisional.
Cicatrización de la herida excisional: Durante la cicatrización ósea, ocurren los mismos eventos de inflamación, fibroplasia y remodelado, anteriormente explicados para los tejidos blandos, la diferencia radica en la presencia de osteoblastos y osteoclastos encargados de reconstituir y remodelar el tejido calcificado.15
La herida excisional incluye al hueso cortical, hueso alveolar, endostio, ligamento periodontal, cemento y dentina.11 Siendo el ligamento periodontal, el que posee mayor capacidad de regeneración en comparación con los otros tejidos del periodonto.7 Todos estos tejidos a excepción de la dentina, tienen capacidad de regeneración. A menudo, esta herida mide centímetros de diámetro la cual debe ser rellenada por un coágulo que no promueve la cicatrización, sino por el contrario, actúa como una barrera que deberá ser removida antes de que la cicatrización pueda progresar.11,12
Al segundo o cuarto día después de ocurrida la herida, se puede observar el comienzo del proceso de cicatrización; el tejido proliferativo encapsula la raíz resecada e inicia la reformación del aparato dentoalveolar. Este tejido de granulación proviene del ligamento periodontal y endostio y es el principal responsable de la reparación inicial de la herida excisional en una cirugía endodóntica.11
El proceso de reparación continúa por varios meses después de que la cicatrización mucoperióstica ha terminado y después de 16 a 20 semanas, la fase de maduración y remodelado se ha completado.11
A diferencia de la herida incisional y diseccional, en la cicatrización de la herida excisional, los bordes no pueden ser reaproximados debido a que estos tejidos fueron removidos intencionalmente. En el lugar de la herida excisional se forma un coágulo que actúa como una barrera la cual debe ser removida y reemplazada por un tejido de granulación que migra desde el endostio.40
La cicatrización de la herida excisional tiene dos componentes, la cicatrización dentoalveolar y la ósea. Estos componentes inicialmente son independientes uno de otro, pero a medida que el proceso de cicatrización avanza, la cicatrización dentoalveolar depende de la ósea.31,41
Cicatrización dentoalveolar apical: Aunque la secuencia exacta de los eventos que ocurren durante la cicatrización dentoalveolar apical, no se conocen todavía, se cree que las células ectomesenquimatosas indiferenciadas pluripotenciales que provienen del ligamento periodontal y del endostio, se diferencian en fibroblastos, osteoblastos y cementoblastos, para sintetizar sustancia fundamental y colágeno, hueso y cemento nuevo, respectivamente.11
Al transcurrir 10 a 12 días, los cementoblastos comienzan a depositar cemento sobre la superficie resecada de la raíz;11,12 mientras que los osteoblastos comienzan a formar hueso entre el décimo y décimo cuarto día. A los 28 días, se puede apreciar una pequeña capa de cemento que cubre casi la totalidad de la superficie dentinaria resecada y trabeculado óseo en la periferia de la cavidad. También se pueden observar fibras colágenas orientadas paralelamente a la raíz resecada. Estas nuevas fibras del ligamento periodontal muestran evidencias de funcionalidad.11
Después de 8 semanas, la raíz resecada (más no el conducto radicular), muestra una cobertura completa de cemento y el trabeculado óseo se observa más denso y con abundantes osteoblastos. Para este momento muchas de las fibras del nuevo ligamento periodontal, se encuentran orientadas funcionalmente entre el cemento y el hueso, a excepción de las fibras adyacentes al conducto radicular y al material obturador las cuales mantienen su orientación paralela.11
Finalmente a las 16 semanas después de realizada la cirugía, el aparato dentoalveolar apical se observa muy similar al normal.11
Algunos estudios han reportado evidencia de resorción dentinaria y cementaria.11,42,43 Pero aparentemente esta resorción es ocasional y ligera.43 La formación del nuevo cemento puede ser sobre el cemento viejo, la dentina o cemento y dentina.36,43 El nuevo cemento puede ser acelular o celular.36,43,44
Después de un procedimiento de instrumentación mecánica se forma una capa de desecho, compuesta por material orgánico e inorgánico.12 Esta capa de desecho actúa como una barrera para la unión del nuevo tejido conjuntivo con el cemento.12,45
La cicatrización dentoalveolar apical, ocurre a un menor ritmo en comparación con la cicatrización ósea.31 Al parecer, este proceso se puede acelerar si la raíz resecada se desmineraliza con ácido cítrico.11,12,23,25,31,41,43,45,46
Existen estudios que han demostrado que la unión de las fibras colágenas al cemento radicular es más fuerte y rápida si la dentina es acondicionada con ácido cítrico11,12,23,25,41,43,45,46 y tetraciclina,23 para eliminar la capa de desecho,12,45 además de aumentar la cicatrización y ayudar a la formación de un aparato dentoalveolar apical funcional.11,12,41
Garrett y Stahl et al. citados por Karring, Lindhe y Cortellini 23 sugirieron que la desmineralización de la superficie radicular con exposición del colágeno dentinario, podía facilitar el depósito de cemento mediante inducción de las células mesenquimáticas del tejido adyacente para que se diferenciaran como cementoblastos.23,45
Así mismo, Polson, Ladenheim y Hanes 45 concluyeron que en su estudio hubo marcadas diferencias in vivo entre el grupo control (sin tratamiento de ácido cítrico) y el experimental (con tratamiento de ácido cítrico). Ellos realizaron el estudio en dientes de humanos con enfermedad periodontal que fueron extraídos, tratados o no con ácido cítrico e implantados en la piel del dorso de ratas.
En el grupo experimental, se observó un número significativamente mayor de células de inserción en comparación con el grupo control. Este hallazgo coincidió con otros estudios in vitro e in vivo. La inserción de las fibras ocurrió 5 a 10 días después de la implantación.45
Pero en el estudio de Bogle et al. citado por Karring, Lindhe y Cortellini 23 se evidenciaron varios especimenes con anquilosis y resorción radicular después de tratar con ácido cítrico las furcaciones de dientes de perro.
Las raíces resecadas no desmineralizadas en el estudio de Harrison y Johnson 41 evidenciaron actividad osteoclástica y aposición de cemento en forma de cuña; es probable que esto no ocurriera si se hubiera desmineralizado la superficie.
Craig y Harrison 12 realizaron una investigación en raíces resecadas de dientes de perros; ellos trabajaron con dos grupos, uno experimental al cual se les desmineralizó la raíz con ácido cítrico al 50% con un pH de 1, por 2 minutos y otro estándar que no recibió tratamiento con el ácido cítrico.
En el grupo experimental se observó aposición de cemento a los 12 días, a los 16 días el cemento recubría aproximadamente el 50% de la superficie resecada, mientras que el grupo estándar no mostró reparación del cemento a los 16 días incluso hasta los 45 días después y cuando éste fue observado, recubría menos del 50%. Posteriormente a los 45 días, se observó reformación del aparato de inserción y cicatrización dentoalveolar del grupo experimental; el grupo estándar no mostró estos mismos resultados.12
Por el contrario, Andreasen 44 encontró aposición de cemento en la periferia de las raíces resecadas con progresión hacia el conducto radicular sin desmineralizar la superficie de la raíz.
La aposición de cemento es considerada como un paso crítico para la cicatrización dentoalveolar, la presencia de la capa de desecho puede interferir con la reparación del cemento y por consiguiente puede afectar la cicatrización.12
Según Egelberg citado por Harrison y Johnson 41 se presume que la actividad osteoclástica en el cemento y dentina, ejercen la misma función que el procedimiento de desmineralización con ácido cítrico, que es exponer la matriz colágena para aumentar la pronta aposición de cemento.
Bajo condiciones ideales la cicatrización de la herida excisional culmina en una reformación del aparato de inserción apical 12,41,47 y aposición de cemento sobre el material de obturación a retro.31,47 Ésta es una característica que pocas veces se ha observado en los materiales convencionales de obturación a retro, pero ha sido detectada rutinariamente en los estudios con Agregado Trióxido Mineral (MTA).31,48-50
El tejido responsable de la cicatrización dentoalveolar es el que encapsula a la raíz resecada, el cual prolifera desde el ligamento periodontal. Este tejido tiene la capacidad genética de formar las estructuras necesarias, tales como, cemento, hueso alveolar, fibras colágenas.12,41
Cicatrización ósea: Existen muchos puntos de controversia acerca de los aspectos generales de la reparación ósea. En la actualidad se pone un gran énfasis en la investigación de la fisiología y la fisiopatología del hueso.16
Para el proceso de cicatrización ósea, también se pueden utilizar los términos de cicatrización por primera y segunda intención. La cicatrización por primera intención ocurre cuando existe una fractura incompleta y los bordes de la misma no se encuentran separados o cuando los extremos de la fractura son reaproximados y rígidamente estabilizados por el cirujano. Por el contrario, si los bordes se separan un milímetro o más la cicatrización será por segunda intención.15
Cuando la cicatrización es por primera intención, se produce un pequeño tejido fibroso que rápidamente se osifica con una mínima formación de callo.15 El callo es la estructura que une a los extremos fracturados del hueso el cual está compuesto de cantidades variables de tejido fibroso, cartílago y hueso.9,16 Si los bordes están separados, la cicatrización por segunda intención provocará la formación de mayor cantidad de tejido fibroso y por consiguiente un callo más grande,15 (Gráfico 44).
Cuando un hueso se fractura los vasos haversianos del hueso y de la cavidad medular que cruzan la línea de fractura se rompen y el periostio y endostio se desgarran. Debido a la rotura de los vasos, se extravasa sangre y al mismo tiempo hay pérdida de la circulación y falta de abastecimiento sanguíneo local; por lo tanto, los osteocitos y la médula ósea mueren. El hueso muerto se extiende varios milímetros más allá de la línea de fractura.9,16
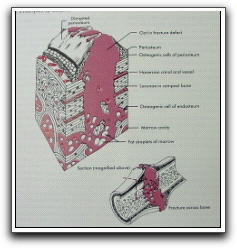 |
Gráfico 44. Fase temprana de la etapa fibroplástica de la reparación ósea. Las células osteogénicas derivadas del periostio y médula, proliferan y se diferencian en osteoblastos, osteoclastos y condroblastos y los capilares comienzan a crecer. Tomado de Peterson et al. 1998. |
En los casos de fracturas óseas, en poco tiempo las células progenitoras del endostio y las células multipotenciales de la médula ósea invaden el coágulo y forman un callo interno. Entre tanto, en los extremos de la fractura, se forma un callo externo que conduce a la unión de ambos fragmentos,9,16 (Gráfico 45).
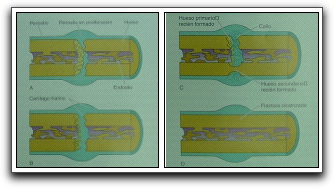 |
|
|
Gráfico 45. Esquema de los fenómenos que ocurren en la reparación de una fractura ósea. Tomado de Gartner y Hiatt 2002.. |
El tejido conjuntivo fibroso o callo que se forma en el sitio de la fractura requiere de un alto grado de vascularización para que finalmente ocurra la osificación. Si el suministro de oxígeno está comprometido se formará cartílago en lugar de hueso.9,15,16 Este cartílago posteriormente se calcificará y será sustituido por hueso esponjoso que luego se remodelará,9 (Gráficos 46 y 47).
A los 4 días después de ocurrida la lesión, el endostio que recubre el trabeculado óseo en las profundidades de la herida excisional comienza a proliferar y migra hacia el coágulo. Poco tiempo después, el endostio además de recubrir el interior de la herida protege al tejido de granulación y encapsula el final de la raíz. Las células involucradas en este tejido son las células ectomesenquimatosas indiferenciadas, las células osteoprogenitoras, los preosteoblastos y los osteoblastos.11
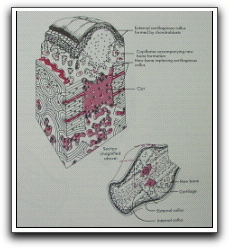 |
Gráfico 46. Fase tardía de la etapa fibroplástica de la reparación ósea. Osteoclastos reabsorben el hueso necrótico. En las áreas de suficiente tensión de oxígeno, los osteoblastos colocan nuevo hueso; mientras que en las áreas con baja tensión de oxígeno, los condroblastos colocan cartílago. También continúa el crecimiento capilar y la formación de los callos internos y externos. Tomado de Peterson et al. 1998. |
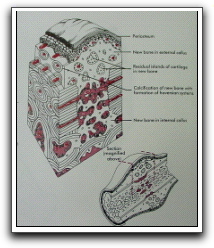 |
Gráfico 47. Etapa de remodelado de la reparación ósea. Los osteoclastos remueven el hueso innecesario y los osteoblastos colocan nuevo tejido óseo. Se desarrollan nuevos sistemas haversianos. Se depositan capas concéntricas de hueso cortical a lo largo de los vasos sanguíneos. Gradualmente los callos disminuyen de tamaño. Tomado de Peterson et al. 1998. |
Tan sólo a los 6 días después de la cirugía comienza la formación de hueso.11 Los bordes de la herida excisional se encuentran desvitalizados y por lo tanto las lagunas de la periferia se observan vacías,40 para el duodécimo y decimocuarto día ya presenta abundantes lagunas con osteocitos11 y el hueso medular ocupa casi la totalidad del defecto óseo.40 Entre la tercera y cuarta semana se ha observado que 3/4 a 4/5 de la herida se encuentran rellenos de trabeculado óseo11 con un periostio activo reparando la tabla cortical.40
Es interesante que la aposición del hueso nuevo durante la cicatrización de la herida excisional, sea directamente sobre la cortical y el hueso medular desvitalizado. En contraste, durante la cicatrización de la herida diseccional, inicialmente se observa actividad osteoclástica antes de la osteoblástica debido a que no ocurre aposición ósea sobre el tejido desvitalizado.40
En la octava semana disminuye el número de osteoblastos activos y el trabeculado óseo se aprecia más denso y abundante, el cual comienza a ser reemplazado por hueso laminar maduro. Para este momento, el endostio se puede observar idéntico al normal. El proceso de cicatrización de la herida excisional progresa desde la cara interna de la herida hacia la superficie externa ósea y es el endostio el principal responsable de la reparación ósea durante las primeras 8 semanas.11
La reparación completa de la herida excisional, excepto la cortical ósea, es apreciable en la semana 16. El período de tiempo exacto necesario para que la tabla cortical complete su reparación es todavía desconocido.11
La cicatrización del hueso alveolar es variable, debido a que algunas zonas presentan una delgada capa de hueso que limita la capacidad de regeneración. En cuanto al hueso esponjoso o medular y al hueso cortical, tienen buena capacidad de reparación; pero si ambas corticales, vestibular y lingual, son destruidas la reparación deja una cicatriz que trae como consecuencia la persistencia en la radiografía de una imagen radiolúcida.7,51-53
La cicatrización de la herida excisional se puede determinar en una radiografía evaluando la cantidad de regeneración ósea aparente.11,31,38,51,54 Pero aunque el examen radiográfico revele cicatrización ósea, es todavía menos capaz de revelar la curación dentoalveolar apical.31
En los casos de destrucción considerable de la cortical vestibular y lingual, usualmente no se completa la regeneración ósea y por lo tanto se desarrolla un denso tejido conjuntivo fibroso, lo que trae como consecuencia la formación de una cicatriz.11,38,51,52,55
Desde el punto de vista histológico, la cicatriz apical está compuesta por una masa densa de tejido conjuntivo fibroso con gruesos haces de colágeno y fibrositos fusiformes. En ocasiones se encuentran algunas células inflamatorias crónicas.38
Rud, Andreasen y Jensen 51 refieren que este fenómeno fue descrito en 1933 por Hammer y es común observarlo en los laterales superiores y no es un indicativo de fracaso endodóntico sino más bien otra forma de cicatrización.11,38,51,53,55,56
Existe una teoría que trata de explicar la etiología y patogénesis de una cicatriz apical; se piensa que los cambios inflamatorios y la interrupción de la función del diente podría impedir la cicatrización.55
Por otro lado, Baek y Kim 57 refieren que probablemente debido a la lenta regeneración del hueso en comparación con los tejidos blandos, la cavidad ósea es ocupada por tejido blando por lo cual se forma un tejido cicatricial fibroso. Si este tejido fibroso se establece primero en la cavidad, es probable que actúe como una barrera que puede obstaculizar la formación de hueso.56,57
Rud, Andreasen y Jensen 51 encontraron con mayor frecuencia la formación de cicatriz apical en los pacientes comprendidos entre 20 y 49 años de edad. También observaron que los dientes con evidencia radiográfica de periodontitis apical crónica (para el momento de la cirugía), eran más propensos a presentar inflamación periapical en los controles postoperatorios.
La cicatrización ósea es producto de la proliferación del endostio.12,16 En un estudio en el cual a un grupo se le realizó desmineralización de la superficie radicular y al otro no, se observó que la cicatrización progresó en ambos, indicando que la cicatrización del hueso no depende completamente de la cementogénesis.12
En conclusión, la cicatrización ósea idealmente culmina con la reformación del trabeculado y cortical. El tejido responsable de esta cicatrización es el endostio el cual prolifera del endostio de los bordes de la herida excisional. Este tejido también contiene la información genética para formar hueso nuevo.12,41
Harrison y Jurosky 40 concluyeron que durante la cicatrización ósea de la herida excisional, el hueso nuevo se depositó directamente sobre la superficie del tejido desvitalizado; no se observó actividad osteoclástica; el endostio fue el principal tejido involucrado en la cicatrización y el periostio no tuvo función en la reparación ósea hasta que la herida excisional estuvo casi completamente rellena con hueso esponjoso nuevo.
Sin embargo, la cicatrización ósea no termina con el relleno completo del defecto en el hueso, el hueso recién formado tiene que ser remodelado y madurado para alcanzar el aspecto característico del sitio en cuestión.58
Proceso de cicatrización según el procedimiento quirúrgico endodóntico realizado
La cicatrización después de un procedimiento quirúrgico endodóntico depende de varios factores: edad, diente tratado, material de obturación a retro, la presencia de quistes o granulomas, inflamación aguda o crónica, resección radicular o legrado apical, entre otros. Sin embargo, resulta extremadamente difícil determinar estadísticamente la influencia individual de cada factor.51
Andreasen y Rud 55 realizaron la evaluación histológica de 70 cirugías periapicales efectuadas en humanos, en un período postquirúrgico de 1 a 14 años. Ellos observaron que la cicatrización después de una cirugía periapical podía ser de tres tipos.
Cicatrización con nueva formación del ligamento periodontal o anquilosis, acompañada de ninguna o ligera inflamación periapical; cicatrización con presencia de tejido fibroso (cicatriz) en comunicación o adyacente al ligamento periodontal, anquilosis ocasional y varios grados de inflamación; y por último, inflamación periapical moderada a severa sin cicatriz apical. En el 7% de los casos se observó anquilosis entre la superficie radicular y el hueso alveolar.55
Durante la cicatrización después de una cirugía periapical, debería haber regeneración de todos los componentes periodontales: cemento, ligamento periodontal y hueso.55
La cicatrización periapical y radicular después de una resección apical
La resección radicular es la remoción quirúrgica de una porción del ápice radicular de un diente, este procedimiento expone la dentina, el cemento y el conducto radicular. El desenlace de este procedimiento depende de la reacción del tejido conjuntivo que entra en contacto con estas superficies expuestas.59
En la mayoría de los casos la resección radicular se ejecuta en presencia de una inflamación crónica periapical, la cual involucra al cemento y dentina. Al parecer, si los túbulos dentinarios se encuentran contaminados con bacterias no se podrá depositar nuevo cemento sobre esta superficie.59
Coolidge 59 en 1930, reportó un caso de un primer premolar superior que presentaba tratamiento de conducto previo obturado con gutapercha, con una gran imagen apical, al cual se le realizó una resección apical; 14 años después del procedimiento quirúrgico, la evaluación radiográfica demostró que el área que anteriormente había estado ocupada por un granuloma, se encontraba completamente rellena con hueso nuevo y rodeada por el espacio del ligamento periodontal normal.
Posteriormente, el diente fue extraído y se realizó la evaluación histológica del mismo. La cual evidenció aposición de nuevo cemento que cubría la totalidad de la longitud de la superficie expuesta. No se observaron células inflamatorias en los tejidos adyacentes a la obturación del conducto o la superficie resecada.59
Así mismo, en el estudio de Andreasen y Rud 55 se observó formación de nuevo cemento en las zonas periféricas de la superficie radicular resecada, lo que sugiere que éste se origina de las porciones laterales intactas de la raíz. Csernyei en 1932 y Hoenig en 1935, citados por Andreasen y Rud,55 también observaron partes de la raíz resecada cubiertas de cemento nuevo. La regeneración del ligamento periodontal, usualmente consistió en la formación de una cápsula fibrosa que recubría el final de la raíz. 55
Svejda y Brazda 60 realizaron una investigación bajo microscopio electrónico de barrido de las superficies radiculares de 8 dientes humanos que recibieron una resección apical. Sus hallazgos demostraron aposición de nuevo cemento, algunas lagunas de resorción y desarrollo de un nuevo ligamento periodontal sobre la superficie resecada.
Bauer en 1925 citado por Coolidge,59 reportó completa cicatrización del hueso, ligamento periodontal y aposición de nuevo cemento, pocos meses después de realizar resecciones apicales en dientes de animales.
Persson citado por Hirsch et al.61 observó en su estudio, que la cicatrización periapical después de una apicectomía en dientes con quistes apicales tendía a ser mejor en comparación a los casos que presentaban tejido de granulación.
Hirsch et al. 61 basados en los criterios radiográficos propuestos por Rud, Andreasen y Jensen,62 observaron que los casos con destrucción periapical menor o igual a 5mm, tenían mejor pronóstico que las lesiones más grandes. Además, el porcentaje de defectos cicatrizados fue bajo (46,7%); al parecer esta baja tasa de cicatrización completa, se relacionó con los períodos de observación postoperatorios que fueron realizados a los 24 y 36 meses.
Debido a que los fracasos endodónticos se relacionan con la inadecuada limpieza y conformación del sistema de conductos radiculares y la salida de irritantes hacia los tejidos periapicales,27,63 se ha recomendado la colocación de una obturación a retro en los dientes que requiere una resección apical.63
La cicatrización periapical y radicular después de una resección apical y obturación a retro
La resección y obturación apical a retro tienen como objetivo, lograr un sellado impermeable que evite la salida de cualquier agente nocivo, real o potencial, desde el sistema de conductos radiculares hacia los tejidos perirradiculares.63-65
Al realizar una apicectomía se remueven hueso y cemento necrosados 52 y los irritantes provenientes de los conductos radiculares,33,34 lo que facilita el proceso de reparación.33,34,52
Los materiales de obturación a retro son variados, se han propuesto la gutapercha, resina compuesta, ionómeros de vidrio, amalgama, cementos de ácido ethoxybenzoico (EBA), cementos de policarboxilato, cavit, cementos de óxido de zinc, entre otros.33,47
Hasta ahora ninguno de estos materiales ha demostrado predeciblemente la regeneración del periodonto a todo lo largo de la superficie radicular.47 Recientemente el MTA se ha sugerido como un material potencial de obturación apical a retro.28,47-50,63,66-69 Ya que experimentalmente se ha observado aposición de cemento sobre la superficie resecada y este material obturador.48,63
Los estudios clínicos generalmente se refieren al uso de la amalgama como material de obturación a retro.31,63 Aunque recientemente ha habido interés en buscar materiales alternativos a la amalgama debido a que ésta posee una pobre capacidad de sellado, alto potencial de corrosión, sensibilidad a la humedad, pigmentación de los tejidos duros y blandos, toxicidad y tasa de éxito clínico baja.63,70,71
En un estudio en el cual se evaluaron 1.000 dientes tratados quirúrgicamente, se observó que aquellos dientes que presentaban obturaciones a retro de amalgama, fracasaron cuatro veces más que los dientes obturados de manera ortógrada con gutapercha (83% de completa cicatrización).72 Aparentemente la tasa de éxito de los dientes obturados a retro con amalgama es menor que los obturados de forma convencional con gutapercha.71,73,74
Pitt Ford et al.73 observaron que después de reimplantar dientes de monos a los cuales se les realizaron apicectomías y obturaciones apicales a retro con IRM (Material de Restauración Intermedio) o amalgama, el 60% de los obturados con IRM presentaron inflamación apical con extensión no mayor a 0,1mm alrededor de la raíz; mientras que en el 92% de los obturados con amalgama se evidenció inflamación de moderada a severa y el 67% mostró una extensión mayor a 0,5mm.73
La respuesta tisular al material de obturación a retro IRM después de 2 meses, fue significativamente menos severa y extensa que la observada con la amalgama. Por lo tanto, el éxito de una obturación a retro de amalgama en dientes reimplantados debería estar cuestionado.73
En un estudio posterior, Pitt Ford et al.70 examinaron histológicamente el efecto de varios cementos a base de óxido de zinc y eugenol como materiales de obturación a retro en dientes de monos reimplantados. Se concluyó que la respuesta tisular del IRM, IRM con virutas de dentina, SuperEBA y Cavit, fue menos severa que la observada con un cemento de óxido de zinc y eugenol, y Kalzinol. Pero todos estos materiales tuvieron una respuesta tisular más favorable que la amalgama.
La agregación de virutas de dentina al IRM se realizó en una tentativa de inducir la aposición de cemento sobre la superficie de la raíz obturada a retro. Aunque ningún espécimen exhibió tal respuesta,70 la aposición de cemento ha sido observada en otros estudios.31,44,48,49,59,63
También se ha observado en otros estudios que la obturación retrógrada con amalgama generó más resorción radicular que la obturación retrógrada con gutapercha.75,76
El IRM o material de restauración intermedia, ha sido recomendado como material para obturar a retro cavidades en endodoncia debido a su biocompatibilidad, integridad marginal y reportes de éxito.41,73,74 Estudios clínicos recientes indican que el IRM es significativamente más exitoso que la amalgama,73,74 aparentemente la amalgama no permite una adecuada cicatrización debido a que no provee un adecuado sellado a las bacterias.73
Dorn y Gartner,74 evaluaron radiográficamente en un período de 6 meses a 10 años postquirúrgicos, 488 casos que recibieron cirugías apicales, los resultados arrojaron una tasa de éxito con SuperEBA de 95%, IRM 91%, y amalgama de 75%. No hubo diferencias estadísticas significativas entre el IRM y SuperEBA.
En un estudio se realizó la evaluación radiográfica y microscópica de dientes de perros que recibieron cirugías apicales que incluían la resección apical con obturación ortógrada de gutapercha y resección apical con obturación a retro de IRM o amalgama; el período de evaluación fue de 10 a 45 días.41
Los resultados mostraron que no hubo inhibición de la cicatrización ósea ni dentoalveolar asociada a estos materiales. Pero hay que considerar que el procedimiento fue efectuado en animales, con controles postoperatorios muy cortos (10 a 45 días) y sin lesiones perirradiculares previas a la cirugía. Además, estos estudios en animales de experimentación han demostrado una rápida cicatrización ósea,12,41 mientras que el ritmo de cicatrización de este tejido en los seres humanos, aún no se ha podido determinar por completo.41
El uso de IRM como material de obturación a retro ha demostrado éxito clínico,74,77 y ha exhibido una aceptable reparación del tejido periapical.41
Últimamente el uso de los cementos a base de óxido de zinc y eugenol para obturaciones a retro han sido ampliamente difundidos; lo que aparentemente ha contribuido a aumentar los índices de éxito,31,74 aunque en otros estudios esto no se ha podido demostrar.31,78,79
El objetivo final después de realizar una resección y obturación retrógrada apical, es lograr la cicatrización del aparato de inserción apical,12,41,47 la cual incluye la aposición de cemento sobre el material de obturación a retro.31,47 Ésta es una característica que pocas veces se ha observado en los materiales convencionales de obturación a retro, pero ha sido detectada en los estudios con Agregado trióxido Mineral (MTA).31,48-50,63
Torabinejad et al.63 evaluaron en perros, la respuesta de los tejidos periapicales después de realizar cavidades a retro y obturarlas con MTA y amalgama. La evaluación histológica después de 10 y 18 semanas evidenció, que los casos obturados con MTA presentaban menor extensión y severidad de la inflamación, mayor aposición ósea y frecuente aposición de cemento sobre el material.
En otro estudio también realizado por Torabinejad et al.48 en perros, el examen histológico de los tejidos periapicales 5 meses después de haber realizado obturaciones a retro con MTA y amalgama, demostró la formación de una capa completa de cemento sobre el MTA en todos los especimenes evaluados. También se evidenció ausencia de inflamación en el 83% de los casos obturados con MTA.
Al parecer la capacidad de sellado y adaptación marginal del MTA es superior a la amalgama, IRM y SuperEBA.69 Aunque el mecanismo de formación del cemento sobre el MTA no está muy claro, al parecer, el MTA activa a los cementoblastos, lo que podría inducir la cementogénesis.80
Andreasen 44 fue el primero en reportar el modelo de aposición del cemento en superficies radiculares no desmineralizadas resecadas;41 él evaluó en un estudio histológico, la discrepancia que podía existir durante la reparación del cemento después de un procedimiento quirúrgico endodóntico. En este estudio no solo trabajó con dientes resecados y obturados a retro, sino que también utilizó dientes a los cuales sólo se les realizó la resección apical.44
Durante esta evaluación histológica él encontró que el tejido blando adyacente a la superficie del cemento podía ser de siete tipos, (Gráfico 48). En el tipo 1, el ligamento periodontal se encontraba funcional y fue asociado con una densa capa de cemento eosinófilo, a menudo de tipo celular. La presencia de fibras colágenas sin disposición funcional (tipo 2 y 3) exhibían una pequeña cantidad de cemento eosinófilo, usualmente de tipo acelular.44
Finalmente, la presencia de tejido fibroso cicatricial, tejido de granulación inflamatorio, tejido conjuntivo o epitelio (tipo 4 a tipo 7), fue asociado con marcada disminución en la cantidad de cemento reparado. En los casos en los que se pudo observar cemento, fue de tipo basófilo (probablemente por la aposición lenta), aunque en muchos casos la superficie resecada no mostró cemento reparado por completo. También se pudo observar que el tejido cicatricial, presentaba una menor cantidad de células en comparación al ligamento periodontal.44
Es por esto que Andreasen 44 concluyó que existió una asociación importante entre el cemento reparado y la formación de fibras periodontales funcionales. Por lo tanto, este hallazgo apoya a la creencia de que la función principal del cemento radicular, es el anclaje de las fibras del ligamento periodontal y sí las fibras no están presentes, el cemento no es aprovechado.
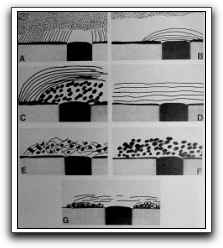 |
Gráfico 48. Dibujo esquemático que ilustra la clasificación del tejido blando adyacente a la superficie radicular. A, Tipo 1: Fibras colágenas que se extienden del cemento al hueso. B, Tipo 2: Fibras colágenas que se extienden de cemento a cemento. C, Tipo 3: Fibras colágenas que se extienden del cemento a la periferia de un granuloma o quiste. D, Tipo 4: Fibras colágenas paralelas a la superficie radicular. E, Tipo 5: Tejido conjuntivo con inflamación. F, Tipo 6: Tejido de granulación con inflamación. G, Tipo 7: Proliferación de epitelio en la superficie radicular. Tomado de Andreasen. 1973. |
Esto pudiera explicar porque algunos dientes incluso varios años después, en presencia de tejido cicatricial, no muestran reparación del cemento por completo. Aparentemente, el tipo de disposición de las fibras del ligamento periodontal, también tiene importancia.44
La cicatrización periapical y radicular después de un reimplante
El reimplante se define como la colocación de un diente en su alvéolo nuevamente después de su extracción deliberada o traumática. La extracción deliberada y recolocación se conoce como reimplante intencional.81,82 Así mismo, Grossman 83 indica que es el acto de extraer deliberadamente un diente después de realizar el examen, diagnóstico, tratamiento de conducto y restauración, para finalmente regresarlo a su alvéolo original.
La extracción y reimplante intencional de los dientes, se practica desde hace 1000 años.84 Aunque no es considerado el tratamiento de elección para un diente con periodontitis apical, es un tratamiento de último recurso cuando la terapéutica convencional, el retratamiento o la cirugía son imposibles.31,82,84
Dryden y Arens 84 refieren que la necesidad de realizar reimplantes intencionales se ha reducido por los avances en los materiales endodónticos, aditamentos, técnicas y refinamiento en las habilidades quirúrgicas.
Pero incluso aún con estas mejorías, existen dientes que no cicatrizan y pacientes que se resisten a aceptar la pérdida de un diente, por lo tanto, el reimplante intencional es una alternativa de tratamiento.84
Los acontecimientos histológicos de la cicatrización después de reimplantar un diente, al cual se le han hecho todos los esfuerzos para mantener vital al ligamento periodontal, comienzan desde el mismo momento de efectuarse la reimplantación.85
La cicatrización periodontal después de un reimplante involucra dos estructuras: la porción cementaria del ligamento periodontal a lo largo de la superficie radicular y la porción alveolar del ligamento que se corresponde con el alvéolo.86
Uno de los estudios de Andreasen 86 demostró que la condición de la porción cementaria del ligamento periodontal, es un factor decisivo y determinante para la reparación periodontal después de un reimplante. Aparentemente la porción alveolar del ligamento no tiene influencia sobre la cicatrización periodontal.
A las 24 horas, se pueden observar las fibras del ligamento con severa interrupción en su continuidad y las fibras transeptales con marcada acelularidad, presencia de fibrina y leucocitos polimorfosnucleares.46,85
Después de 3 a 4 días, muchas áreas del ligamento periodontal muestran hialinización y ausencia de células en las porciones cementaria y alveolar; en contraste, en la zona transeptal ocurre una repoblación celular. Tampoco es evidente el suministro sanguíneo en los vasos de la porción que mira hacia el cemento, se pueden observar osteoclastos.46,85
Para la primera semana, la inserción gingival y la población celular del área transeptal aparece completa, pocas áreas del ligamento periodontal muestran fibras principales reparadas, pero se hace evidente la circulación sanguínea en las porciones cementaria y alveolar del ligamento periodontal. También pueden observarse áreas de resorción superficial e inflamatoria.46,85
Dos semanas después, es casi imperceptible la línea de separación del ligamento periodontal, es frecuente observar a las fibras periodontales principales. Pero para este momento, se evidencian zonas de anquilosis.85
Ya a los 21 días la zona transeptal se encuentra totalmente normal y aunque en el ligamento periodontal son evidentes las células y la restauración de la continuidad de las fibras, está ausente una orientación normal de estas fibras ya que se observan paralelas a la superficie radicular.46 Al transcurrir dos meses, las fibras principales se pueden apreciar normales en cantidad y orientación.85
También son evidentes zonas de resorción tanto del cemento como la dentina, de extensión variable; aunque algunas áreas de resorción demuestran depósitos cementoides. En los espacios medulares son evidentes áreas con formación de hueso nuevo.46
La resorción radicular externa después de un reimplante, se ha dividido en tres tipos: resorción superficial, inflamatoria y por sustitución o anquilosis.85,87
La resorción superficial es consecuencia del daño generado a la capa más interna del ligamento periodontal 81,91,95 y posiblemente también del cemento,31,54,85,88 lo cual desencadena un proceso osteoclástico de leve a moderado sobre la superficie radicular.84,85,88 Este tipo de resorción se puede observar histológicamente una semana después de haber realizado el reimplante. Por lo general no son evidentes radiográficamente,85 y posteriormente se reparan por aposición de nuevo cemento.85,88
También en los casos de reimplante de dientes a los cuales no se les ha realizado el tratamiento de conducto, el daño al ligamento periodontal 85,89,90 y cemento 31,85,89,90 causará resorción radicular que expondrá los túbulos dentinarios. Si se ejecuta el tratamiento de conducto o si el estímulo bacteriano es débil, la resorción remite; de lo contrario, la resorción continuará hasta que el tejido de granulación entre en contacto con el conducto.85,89,90
Este tipo de resorción también es evidente histológicamente una semana después de realizado el reimplante 85 y se caracteriza por áreas de resorción en el cemento y dentina y cambios inflamatorios en el periodonto adyacente.88 Radiográficamente se observa como cavidades o socavados sobre la superficie radicular o el hueso contiguo.85
La resorción por sustitución puede preceder o no a la anquilosis y es el resultado de el daño excesivo al ligamento periodontal85,88 y posiblemente también del cemento.31,85,88 La anquilosis es la fusión del cemento y el hueso alveolar con obliteración del ligamento periodontal6 y es consecuencia de la cicatrización a partir del hueso adyacente.85
Histológicamente la anquilosis se puede demostrar dos semanas después del reimplante. Radiográficamente hay ausencia del espacio del ligamento,85 clínicamente el diente anquilosado es inmóvil y por lo general se encuentra en infraoclusión.88 Al parecer los dientes reimplantados que se anquilosan pierden sus raíces luego de 4 a 5 años.6
También se ha reportado resorción ósea si el compartimiento tisular próximo a la superficie radicular se lesiona. No obstante, esta resorción se detiene y posteriormente es ocupada por hueso neoformado.85 Al parecer el alvéolo juega un papel importante en la cicatrización de los dientes reimplantados.91
En 1955, Hammer citado por Dryden y Arens,84 recalcaba la importancia de dejar el ligamento periodontal intacto en las raíces de dientes reimplantados intencionalmente, debido a que la salud del ligamento era esencial para la reinserción y retención dentaria.
La presencia y vitalidad del ligamento periodontal sobre la superficie radicular del diente reimplantado son decisivas para la cicatrización periodontal.84-87,92,93 Es por esto que se hacen muchos esfuerzos por mantener el ligamento periodontal vital para evitar así las consecuencias más indeseables que son, la resorción radicular externa y la anquilosis.84,86,87,93
Ocasionalmente las raíces extraídas y reimplantadas presentan resorción radicular en la porción apical. Se sugiere que el ligamento periodontal retenido sobre esa parte de la raíz se lesiona durante la extracción, lo cual permite que el hueso o el tejido conjuntivo gingival contacten con la superficie radicular durante la cicatrización y se produzca la resorción.23
Es por esto que al parecer sólo las células del ligamento periodontal son capaces de regenerar el ligamento periodontal perdido.23 También se le ha atribuido al ligamento periodontal vivo de dientes maduros, cierto potencial osteogénico. 85,94
Para prevenir dañar al cemento el diente debe ser extraído cuidadosamente y reimplantado lo antes posible, usualmente a los 15 minutos, la superficie radicular no debe tocarse con las manos.31 Inclusive después de realizar una técnica cuidadosa, histológicamente la resorción inflamatoria 31,70,71,73,87,93 y la anquilosis 86,87,93 han sido complicaciones frecuentes.
También se ha demostrado que el período de tiempo extra alveolar que transcurre antes de reimplantar un diente, ejerce alguna influencia sobre el alvéolo y por lo tanto aumenta las posibilidades de desarrollar una anquilosis.86,87
Si el período extra alveolar es limitado y menor a 2 horas, podrían sobrevivir unas pocas células del ligamento periodontal.86 Pero se ha observado que después de 30 minutos extra alveolares, en un medio de almacenaje seco, la resorción inflamatoria ha sido prominente, mientras que a los 60 minutos, es más eminente la anquilosis.87
Algunos estudios experimentales han demostrado que un período prolongado extra alveolar seco, antes del reimplante, induce resorción radicular extensa.86,87,93
Según Agnew y Fong 95 los criterios para un transplante satisfactorio son, integración orgánica en su nuevo medio; ausencia de lesiones laterales o periapicales discernibles; efectiva función masticatoria; adecuado mantenimiento de las relaciones musculares y oclusales fisiológicas; evidencia clínica y radiográfica de estabilidad que parece compatible con el mantenimiento indefinido del diente y estética aceptable.
Los criterios de curación deben incluir tanto la cicatrización periodontal con respecto a la inflamación periapical como la ausencia de resorción inflamatoria o sustitutiva. Solamente si el diente reimplantado no muestra ningún signo de estas complicaciones, podrá considerarse exitoso el procedimiento.75,76
En la literatura existen muchos reportes de casos, pero en contraste, se dispone de pocos estudios clínicos a largo plazo. La comparación de los estudios es difícil debido a los diferentes métodos de tratamiento y criterios de éxito.31
La tasa de éxito reportada, basados estrictamente bajo el criterio radiológico, es baja, varió desde un 34% a un 67%. 31 Bajo el criterio clínico y radiográfico de 50 a 60%,75 mientas que Emmertsen y Andreasen 76 reportaron un 39 a 62% de curación satisfactoria después de realizar reimplantes intencionales con períodos de observación de hasta 10 a 20 años.
Se consideró que en los casos catalogados como fracasos, la imagen radiolúcida apical persistió o se evidenció resorción radicular.16,31 El tiempo de supervivencia puede variar de 5 a 10 años.75
El pronóstico de los dientes reimplantados depende principalmente de la presencia o ausencia de resorción inflamatoria debido a la reinserción.82,96 También se conoce que el pronóstico del reimplante intencional es mejor en comparación con el reimplante por avulsión.82 Tan solo unos pocos estudios han sido publicados con documentación adecuada de la curación postoperatoria.55,75,76,83
Los resultados del estudio de Proye y Polson 46 indicaron que la cicatrización después de un reimplante ocurre más rápidamente en la zona transeptal que en el ligamento periodontal. Aunque existen estudios como el de Hurst, citado por Proye y Polson 46, que demuestran lo contrario o que indican que ambas ocurren simultáneamente.97 El área transeptal cicatriza similar a la herida incisional y la cicatrización del ligamento periodontal depende primariamente de la repoblación del hueso alveolar adyacente.46
Aqrabawi 82 reportó dos casos clínicos de segundos molares inferiores que presentaban tratamientos de conductos previos y periodontitis apicales crónicas, a los cuales les realizó exodoncia, retropreparación, obturación a retro con amalgama y finalmente reimplante intencional. La última evaluación clínica y radiográfica se realizó 5 años después de ejecutar el procedimiento y ambos casos no mostraron cambios patológicos radiográficos y se encontraban asintomáticos.
Otros autores después de realizar reimplantes en dientes de monos con evaluaciones postoperatorias de 1 día a 4 meses, observaron que la nueva inserción se restauraba después del reimplante. El epitelio proliferó inmediatamente después de realizado el procedimiento y alcanzó su pico máximo al tercer día; al transcurrir siete días el epitelio de unión se reestableció.97
El tejido conjuntivo proliferó y alcanzó su pico a los siete días, para esos días la interface fue indetectable y comenzó a establecerse la continuidad del ligamento periodontal y el tejido conjuntivo supracrestal. La orientación y maduración de las fibras no se pudo observar hasta 4 meses después del reimplante. También fueron apreciables resorciones radiculares y anquilosis a los 14 días de realizado el procedimiento.97
Agnew y Fong 95 llevaron a cabo un estudio histológico de transplantes de dientes de monos en desarrollo, en el cual se pudo observar el desarrollo de un ligamento periodontal altamente celular, funcional y viable. El epitelio gingival y de unión se pereció mucho al de los dientes normales. Estos hallazgos son similares a los pocos estudios histológicos realizados en humanos.16
La cicatrización después de un procedimiento de regeneración tisular guiada
El procedimiento de Regeneración Tisular Guiada (RTG) consiste en colocar una barrera entre la encía y la superficie radicular, para evitar que el rápido crecimiento de las células del epitelio o tejido conjuntivo ocupen el espacio del defecto óseo, durante la fase de cicatrización23,25,57,58,98 para intentar regenerar las estructuras periodontales a través de diferentes respuestas tisulares.13
El principio biológico de la RTG afirma que sólo las células con capacidad para producir regeneración están en condiciones de invadir la lesión tratada quirúrgicamente durante el proceso cicatricial. Esto se logra mediante la colocación de una barrera física que excluya los tipos indeseables de tejidos.23,25,58
Aparentemente las células progenitoras para la formación de un nuevo tejido conjuntivo, residen en el ligamento periodontal. Por consiguiente, se podría esperar que la regeneración de los tejidos del periodonto perdido se alcance si tales células repoblan la superficie radicular durante la cicatrización.23,25
Los resultados de varios estudios sugieren que la exclusión de las células epiteliales y conjuntivas gingivales del área de cicatrización, mediante una barrera física puede permitir (guiar) a las células del ligamento periodontal para que habiten la superficie radicular desprendida.23,25,58
Actualmente existen una gran variedad de membranas bioreabsorbibles y no reabsorbibles,13,23,25,98 con una diversidad de configuraciones destinadas a aplicaciones específicas.23 Las membranas no reabsorbibles deben ser eliminadas de 3 a 6 semanas después de colocadas.23,25,98 Mientras que las bioreabsorbibles, se reabsorben varias semanas después y no requieren de una segunda intervención quirúrgica.23,25
En las últimas décadas, han sido publicados diversos artículos que estudian las posibilidades de aplicación de la RTG.23,31,32,37,56,57,98-103 También se ha podido observar que la colocación de estas barreras o membranas se ha convertido en un tratamiento de rutina en la terapia periodontal.98
Los experimentos en animales, han demostrado que el uso de membranas reabsorbibles y no reabsorbibles producen regeneración del cemento, hueso alveolar y ligamento periodontal funcional.25,57,100
La curación de las lesiones óseas periodontales puede conseguirse predeciblemente de acuerdo con el principio de la RTG, que según varios estudios puede ser aplicada con éxito en otros campos de la Odontología.16,32,56-58,98,99,102
Rankow y Krasner 98 refieren que existen diferentes situaciones clínicas en las cuales se puede aplicar el procedimiento de RTG. Algunas de ellas son, patologías apicales sin comunicación con la cresta alveolar; patologías apicales con comunicación con la cresta alveolar, como por ejemplo las dehiscencias; pérdida ósea radicular o en la bifurcación causada por perforaciones; resorciones radiculares cervicales; fracturas radiculares oblicuas, entre otras.
Por lo tanto, ha sido indicada la aplicación del procedimiento de RTG en los actos quirúrgicos endodónticos, 31,32,37,56,57,98-100,102 ya que puede aumentar las posibilidades de éxito del procedimiento quirúrgico endodóntico.102
Una de las causas de fracaso después de realizar un tratamiento quirúrgico endodóntico o no, es la pérdida de hueso alrededor de la raíz dentaria. Es por esto que la RTG, puede ser adaptada para su uso en cirugía endodóntica.98
Un estudio in vivo realizado en animales evidenció que la regeneración tisular guiada, promovió y aumentó, en la mayoría de los casos, la regeneración del hueso en defectos óseos de origen endodóntico.57 También se ha observado que el uso de las membranas resorbibles en cirugía endodóntica cuando existe un defecto vestibular, aumentó la cantidad de regeneración del hueso alveolar significativamente en comparación con el grupo control en el cual no se utilizó la RTG,100 (Gráficos 49 y 50).
Baek y Kim 57 refieren que en algunos casos a pesar de que el sistema de conductos radiculares se encuentre libre de microorganismos después de un tratamiento endodóntico; la cicatrización ósea no ocurre, debido a que existe un crecimiento del tejido conjuntivo dentro del defecto óseo. El resultado es la formación de una cicatriz periapical, que puede ser erróneamente diagnosticada como una condición patológica.
 |
 |
|
|
|
Es por esto que Pitt Ford 31 refiere que el uso de las membranas permite que la cicatrización ósea ocurra, pero la membrana no tiene influencia sobre la respuesta de los tejidos en el final de la raíz, la cual depende de la exclusión de la infección proveniente del conducto radicular. Por lo tanto se debería realizar una efectiva limpieza, conformación y obturación del sistema de conductos radiculares y una cavidad a retro.
Pecora et al.56 refieren que la colocación de barrera aumentó la cantidad y calidad de regeneración ósea en las lesiones periapicales humanas, ya que aceleró el crecimiento de hueso en las cavidades óseas después de una cirugía endodóntica, (Gráficos 51, 52, 53, 54 y 55).
Maguire et al.101 después de realizar osteotomías, resecciones radiculares y retrobturaciones en gatos, reportaron que en los lugares donde utilizaron membranas reabsorbibles para cubrir el defecto óseo, observaron mayor inflamación adyacente a las raíces resecadas, con diferencias significativas. Así mismo, el uso de las membranas no produjo efectos estadísticamente significativos en la cicatrización ósea o formación de nuevo cemento.
Estos autores argumentan que al parecer las células osteogénicas responsables de la cicatrización ósea de la herida excisional, migran desde los bordes de la herida o defecto en el hueso; si esto fuera cierto, la colocación de una membrana reabsorbible sobre el defecto quirúrgico no debería tener efecto sobre la cicatrización ósea.101
 |
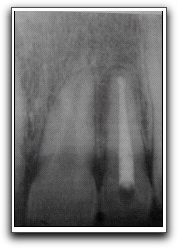 |
|
|
|
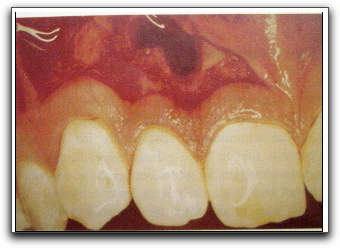 |
|
|
Gráfico 53. Gran lesión periapical en el incisivo lateral superior derecho, seguidamente una cirugía apical retrobturada con un cemento de óxido de zinc y eugenol y colocación de una membrana. Tomado de Pecora, Kim, Celletti y Davarpanah. 1995. |
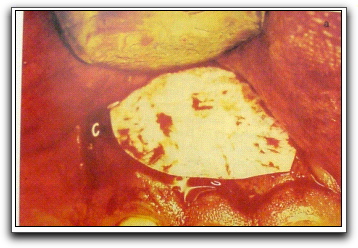 |
|
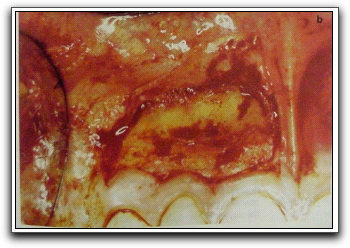 |
|
La cicatrización después de un implante óseo
Es frecuente que, después de una cirugía regeneradora, los defectos óseos no curen o que lo hagan con un tipo de tejido que difiere del original en cuanto a morfología y función (es decir, reparación). Por ejemplo, las lesiones de los maxilares a menudo curan con tejido fibroso en vez de óseo.58
Es por esto que aunque el tejido óseo muestra un gran potencial de regeneración y puede restaurar su estructura y función originales por completo, se puede facilitar o promover la curación, o ambas cosas, colocando materiales de injerto en los defectos del hueso.32,58,104
Los diversos materiales de injertos e implantes se pueden agrupar en cuatro categorías: injertos autógenos, aloinjertos, heteroinjertos o xenoinjertos y los materiales aloplásticos.23,25
Los injertos autógenos, son aquellos implantes óseos transferidos de una posición a otra dentro del mismo individuo; ejemplo de este tipo de injerto son: el hueso tomado de los rebordes edéntulos, tuberosidad maxilar, médula esponjosa ilíaca fresca, entre otros. Los aloinjertos, son injertos transferidos entre miembros de la misma especie, genéticamente diferentes; en este caso el hueso donador es tomado de un cadáver humano.23,25
Los heteroinjertos, se extraen de un donante de otra especie; como por ejemplo, el hueso de ternero, becerro o buey. Mientras que los materiales aloplásticos, son implante inertes utilizados como sustitutos de los injertos óseo; ejemplo de ellos son: el sulfato de calcio (yeso parís), fosfato de calcio (hidroxiapatita) y los derivados del coral.23,25
Las razones para usar injertos óseos o materiales aloplásticos, se basan en la suposición de que el material puede contener células óseo formadoras, también llamadas osteogénicas; el injerto puede servir como andamiaje para la neoformación ósea u osteoconducción, o también que la matriz de los injertos óseos contiene sustancias inductoras de hueso, lo que es conocido como osteoinducción. A menudo los tres mecanismos osteoformadores básicos participan en la regeneración ósea.23,58
El uso de injertos óseos en la terapia periodontal regenerativa se basa en la suposición de que la promoción del nuevo crecimiento del hueso también puede inducir a las células del hueso para que produzcan una nueva capa de cemento con fibras colágenas insertadas sobre superficies radiculares previamente afectadas por periodontitis.23,103
Al parecer, los injertos óseos tienen un efecto regenerador en las grandes lesiones periapicales. Se cree, que el material implantado puede participar en el proceso osteogénico de una forma pasiva.104
Hiatt, Schallhorn y Aaronian 105 evidenciaron en humanos, un 84% de formación de nuevo cemento en casos periodontales donde se colocaron aloinjertos y autoinjertos, mientras que los no injertados solo presentaron nuevo cemento en un 33%. Así mismo, el 85% de los casos que recibieron injertos, presentaron hueso recién formado, en comparación con las zonas no injertadas que solo fue de 33%.
Dragoo y Sullivan 103 realizaron autoinjertos de cresta ilíaca en humanos después de una terapia periodontal inicial y observaron a las 8 semanas, un ligamento periodontal desorganizado, que a las 12 semanas comenzó a mostrar orientación funcional.
A los 8 meses después de realizado el injerto, sin excepción, la evaluación histológica mostró, fibras del ligamento periodontal maduras, funcionales, insertadas en el nuevo cemento y nuevo hueso. La aposición del nuevo cemento se observó a los dos meses y fue de tipo celular; la actividad cementoblástica fue más pronunciada en el segundo y tercer mes, en comparación con el octavo mes de evaluación.103
Varios autores han reportado el aumento en la cementogénesis y osteogénesis en la zona del injerto.32,43,103-106 Estudios histológicos, sugieren que los defectos óseos no injertados, pueden presentar menor relleno óseo, mínima cantidad de nuevo cemento formado, y una unión epitelial larga.43
Lang, Becker y Karring 58 refieren que algunos estudios clínicos y experimentales después de evaluar la colocación de materiales de injertos óseos, observaron que el tratamiento no era predecible y a menudo, los injertos óseos no se unían al sitio injertado y se producía resorción y pérdida ósea asociadas a los procedimientos de injertos.
En estos momentos, la mayor parte de la información sobre los fenómenos biológicos que conducen a la neoformación ósea proviene de estudios con animales. Los resultados concernientes a la formación de hueso obtenidos en estudios con animales tienen que ser aplicados con las debidas precauciones a los seres humanos. En particular, la secuencia cronológica de los diversos pasos que conducen a la formación de hueso mineralizado maduro en el hombre es diferente de la observada con todos los animales de experimentación conocidos.58
Pocas muestras humanas, a menudo en condiciones poco controladas, contribuyen relativamente poco a la comprensión de los fenómenos biológicos de la regeneración ósea en los seres humanos.32,58,104
Aparentemente, los resultados obtenidos con la regeneración tisular guiada mejoran cuando la técnica se combina con injertos colocados en los defectos,25,32,98,102 lo que puede aumentar las posibilidades de éxito del procedimiento quirúrgico endodóntico.102
Dahlin et al. en 1988, citado por Lang, Becker y Karring,58 fueron los primeros en investigar la aplicación del principio de regeneración tisular guiada para la regeneración ósea (regeneración ósea guiada, GBR).
Algunos estudios han demostrado excelentes resultados combinando la aplicación de la membrana no resorbible de politetrafluoretileno expandido (e-PTFE), (Gore Tex Periodontal Material®) con el aloinjerto óseo DFDBA (cresta ilíaca desmineralizada, deshidratada y congelada); pero este procedimiento tiene una desventaja, la membrana no reabsorbible, debe ser removida siempre, por lo tanto se requiere de otra intervención quirúrgica y en algunos casos su remoción es dificultosa.98 Al parecer, los aloinjertos de hueso desecado congelado desmineralizado (DFDBA), facilitan la regeneración en los seres humanos.23
Variables para determinar la cicatrización o no después de un procedimiento quirúrgico endodóntico
El conocimiento de la respuesta de cicatrización es esencial para la evaluación y desarrollo del más efectivo régimen quirúrgico.19 Aunque existe poca información en la literatura científica referente a la cicatrización después de una cirugía periapical, en comparación con los estudios en cirugía periodontal.19,56
La literatura existente en general, ofrece muchas variaciones en los resultados obtenidos después de una cirugía endodóntica. Estas diferencias podrían depender del tipo de criterio aplicado para determinar la cicatrización. Es por esto que la evaluación debe ser cuidadosa ya que existen factores que pueden alterar los resultados, como por ejemplo: el criterio de cicatrización, el período de observación, la selección del caso, el método y tipo de material para la obturación a retro.31,56,61,72,96,107
La cicatrización después de un procedimiento quirúrgico endodóntico, depende de una gran variedad de factores. Pero hay que tomar en cuenta que es difícil obtener de estudios en humanos suficientes controles a largo plazo que permitan un cálculo estadístico, y adicionalmente, varios de estos factores no pueden ser determinados por este método.51
La determinación de la cicatrización debe basarse en la evaluación clínica y radiográfica.37,54,61,96 Pero el criterio clínico de cicatrización, es una evaluación limitada, y en cuanto al examen radiográfico, suponemos que éste refleja los cambios histológicos en la región periapical, aunque no siempre sea así.31,54
De hecho, el proceso de cicatrización completo, varía mucho de un individuo a otro; en algunos se hace evidente radiográficamente en cuestión de meses, mientras que en otros puede transcurrir un año o más hasta que se restablece el patrón trabecular normal.37,38,52
Incluso se han reportado casos que han necesitado hasta 10 años para evidenciarse radiológicamente la resolución completa de la lesión. Debe recordarse que el proceso de cicatrización in vivo va muy por delante de lo que se observa en la radiografía.37,38
Los criterios para valorar la condición periapical después de una cirugía endodóntica, estarán dirigidos a evaluar si la cicatrización fue satisfactoria, incierta o insatisfactoria. Para determinarla, se deben hacer controles postoperatorios a largo plazo, si finalmente el desenlace es un fracaso, se debería considerar el retratamiento quirúrgico o la extracción.62 Se ha reportado en la literatura, que un retratamiento quirúrgico, en la mitad de los casos culmina con una cicatrización completa.108
Rud, Andreasen y Jensen 51 evaluaron la relación entre la variable inflamación y varios factores clínicos como, edad, sexo, tipo de diente, lesión periapical, estado de la infección, diámetro de la cavidad ósea, perforación de la tabla cortical, resección apical, tipo de material de obturación a retro, número de conductos, número de dientes operados, operaciones en dientes vecinos, obturación radicular previa, infección postoperatoria, perno intrarradicular, restauración coronaria, y resorción ósea marginal.
Ellos hallaron que los casos con obturación ortógrada de gutapercha mostraban una significativa menor frecuencia de inflamación que los casos con retrobturaciones con amalgama. Los dientes que presentaban coronas o eran pilares de prótesis fijas, demostraban mayor inflamación (después de un año de control), que los dientes sin estas restauraciones. Para el control final, muchos de los casos que presentaron inflamación periapical, tenían diagnósticos previos de resorción ósea marginal.51
También encontraron menor frecuencia de inflamación periapical en aquellos pacientes que recibieron tratamiento quirúrgico en dos o tres dientes a la vez y en los dientes que no presentaban obturación radicular previa. En los dientes con cavidades óseas de diámetros medianos, se evidenció más frecuencia de inflamación periapical. No se encontró relación entre la variable inflamación y el diente tratado.51
No cabe duda, que la evaluación histológica del área periapical nos proporciona la mejor información acerca de la condición periapical después de la cirugía endodóntica. Desafortunadamente este método de evaluación no puede ser utilizado, y por lo tanto recurrimos al examen clínico y radiográfico.61,62
Debido a la dificultad que existe para correlacionar los hallazgos radiográficos con el estado histológico periapical, Andreasen y Rud 54 en su estudio, trataron de evaluar la conexión que existe entre estos hallazgos.
Después de realizar 70 cirugías periapicales y hacer la evaluación histológica y radiográfica, encontraron, que los casos que presentaban imágenes apicales (mayores al doble del ancho del espacio periodontal normal), a menudo tenían el borde de la imagen apical, circular o semicircular con forma de túnel, e histológicamente presentaban inflamación de moderada a severa. La imagen apical tendía a incrementarse o a permanecer del mismo tamaño. Al parecer el hallazgo radiográfico tenía relación con la situación histológica. Todos los casos sin inflamación o inflamación leve, mostraron disminución del tamaño de la imagen apical.54
En 1972, Rud, Andreasen y Jensen 62 fueron los primeros en proponer una clasificación radiográfica, para valorar la cicatrización periapical después de una cirugía endodóntica, mínimo después de un año postoperatorio.31
Los criterios radiográficos incluían a cuatro grupos: (1) cicatrización completa, (2) cicatrización incompleta (cicatriz apical), (3) cicatrización incierta y (4) cicatrización insatisfactoria (fracaso). Además ellos indicaron que realizar la valoración bajo estos criterios radiográficos, podrían permitir la reproducción de los resultados con cierto grado de precisión.62
Posteriormente, en 1987, estos criterios radiográficos fueron redefinidos por Molven, Halse y Grung, citados por Pitt Ford,31 (Gráfico 56).
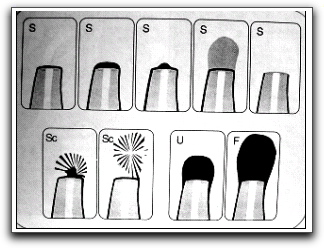 |
|
|
Gráfico 56. Categorías de cicatrización representadas diagramáticamente: hilera superior, varias formas de cicatrización completa (S); hilera inferior cicatrización incompleta, cicatriz (Sc), cicatrización incierta (U), y fracaso (F). (Tomado de Molven et al.) Tomado de Pitt Ford. 1998. |
En un estudio posterior, Molven, Halse y Grung 53 reevaluaron clínica y radiográficamente, casos que después de 2 a 6 años de realizada la cirugía periapical fueron catalogados con cicatrización incompleta. Extendiendo el período de observación a 8-12 años.
Ellos observaron que el 92% continúo catalogado como cicatrización incompleta y solamente un caso que representó el 4% de la muestra, se consideró como un fracaso. Igualmente un solo caso, que representó el 4% restante, cicatrizó completamente después de 8 a 12 años de evaluación postoperatoria.53
Estos autores en ese mismo artículo, ofrecen un dibujo esquemático práctico con basamento científico de cómo determinar radiográficamente la cicatrización en el primer año postoperatorio, después de una cirugía periapical,53 (Gráfico 57).
Para determinar radiográficamente la cicatrización después de una cirugía periapical, existen dos factores que complican la interpretación. El primero es, la presencia de tejido fibroso cicatricial a nivel apical 54 y el segundo factor es, la resección oblicua de la raíz, que hace imposible la evaluación de los cambios adyacentes a la raíz obturada.54,62
Los casos catalogados como cicatrización completa incluyeron, reformación del espacio periodontal (no mayor al doble del ancho normal), presencia de lámina dura alrededor del ápice (se tolera un mínimo defecto a este nivel, pero no mayor a 1mm2), cavidad ósea rellena con nuevo hueso (puede que no tenga la misma radiopacidad del hueso adyacente sano) y en esta categoría también se incluyeron a los dientes que presentaron completa reparación ósea sin espacio periodontal apical apreciable. En este estudio, de 120 casos el 17,5% presentó una completa cicatrización.62
La correlación radiográfica e histológica, en la mayoría de los casos con cicatrización completa, mostraron leve o ninguna inflamación, aunque algunos dientes (24%), mostraron moderada a severa inflamación periapical.62
El grupo con cicatrización incompleta (cicatriz apical), comprendió, a los dientes que presentaron imágenes apicales más pequeñas o del mismo tamaño, en comparación con controles postoperatorios previos; imágenes apicales en las cuales se pudo o no observar estructura ósea en la zona de rarefacción e imágenes de bordes irregulares demarcados con hueso compacto, localizadas asimétricamente alrededor del ápice.53,62 El 23,33% de los 120 casos, cicatrizó incompletamente.62
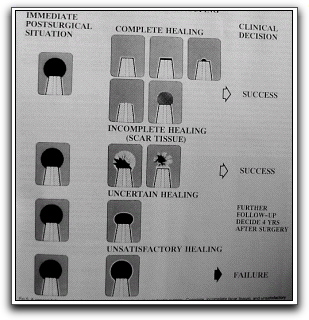 |
|
|
Gráfico 57. Plan de seguimiento general de los casos sujetos a cirugía endodóntica periapical. Cicatrización completa, incompleta (cicatriz apical), e insatisfactoria, se determinan al año de evaluación postoperatorio. La casos con cicatrización incierta se programan para más controles postoperatorios regulares 3 años después para poder clasificarlos como éxitos o fracasados. Tomado de Molven, Halse y Grung. 1996. |
En estos casos hubo correlación entre la cicatrización incompleta y el hallazgo histológico de tejido cicatricial, presentando el 61% severa o moderada inflamación periapical.62
Al evaluar la relación entre la variable de tejido cicatricial y varios factores clínicos, se relacionó a este tejido con los incisivos laterales superiores, probablemente por la cercanía del ápice radicular a la cortical ósea palatina.51,52 Los dientes que presentaron menor incidencia de cicatriz, fueron los caninos y primeros premolares superiores.51
Como se dijo anteriormente, la presencia de cicatriz apical, estuvo relacionada con la perforación de la cortical ósea palatina/lingual,7,51-53 la cual fue más pronunciada en el primer año de control postoperatorio. En cuanto a los dientes con lesiones periapicales (granulomas o quistes), estuvieron también relacionados con la formación de cicatriz apical.51
De los 70 casos tratados quirúrgicamente por Andreasen y Rud,54 35 presentaron en el examen histológico, tejido cicatricial y la frecuencia de éste fue idéntica para los grupos con inflamación leve, moderada o ninguna; mientras que fue menos frecuente en los casos con severa inflamación. En todos los dientes que existió inflamación leve o ninguna y tejido cicatricial, la imagen apical disminuyó de tamaño.54
Las características radiográficas halladas en casos con cicatriz apical fueron: imágenes apicales que tendieron a disminuir de tamaño, de bordes irregulares y de extensión angular en el espacio periodontal, de forma asimétrica con una estructura ósea periférica tosca, sin formación de hueso dentro de la rarefacción.53,54
Radiográficamente es muy difícil determinar si una imagen apical es compatible con una cicatriz sin inflamación, y puede ser confundida a la hora de realizar el diagnóstico, con una inflamación periapical.54
Pero aunque no se puede establecer un diagnóstico definitivo sin examen microscópico, se puede sospechar de la existencia de una cicatriz apical cuando el paciente no presenta dolor ni drenaje, pero se observa una imagen radiolúcida en el ápice de un conducto bien obturado.38
Los casos con cicatrización incierta fueron aquellos que presentaron cierto grado de regeneración ósea e imagen apical más pequeña en comparación a la imagen inicial o a controles postoperatorios previos, el tamaño de la imagen debió ser mayor al doble del espacio periodontal normal, la imagen pudo o no presentar un borde de lámina dura alrededor y los bordes de la imagen casi siempre fueron circulares o semicirculares y simétricos. Otro 23,33% de los 120 casos, se clasificó como cicatrización incierta. Si el caso permaneció como incierto después de 4 años de evaluación postoperatoria, se pudo considerar como un fracaso.62
En el grupo de cicatrización incierta, el 86% mostró severa inflamación periapical y todos los casos insatisfactorios también.62 Además, Rud, Andreasen y Jensen 72 encontraron mayores cambios radiográficos en los grupos con cicatrización incompleta o incierta durante el primer y segundo año postoperatorio.
El último grupo incluyó a los fracasos o a los casos con cicatrización insatisfactoria en los cuales los signos radiográficos de estos casos fueron iguales a los de cicatrización incierta, excepto por el aumento del tamaño de la lesión en comparación con radiografías previas. En este caso el 35,83% se catalogó como fracaso.62
Rud, Andreasen y Jensen 72 basados en los criterios de evaluación radiográfica antes descritos,62 valoraron en un período postoperatorio de 1 a 15 años, 1.000 dientes tratados quirúrgicamente. Observaron que los cambios radiográficos de cicatrización se pudieron observar varios años después de realizada la cirugía.54,72 Grung, Molven y Halse 107 obtuvieron resultados similares.
En contraste, existen autores que una vez clasificados los casos como exitosos o fracasados un año después del procedimiento quirúrgico, no realizaron más controles postoperatorios 77 y aunque para los casos catalogados como cicatrización incompleta, algunos autores recomienda más años de controles,31,51,72 otros indican que un año es suficiente, debido a que al pasar el tiempo, la gran mayoría de estos dientes continúan dentro de la misma clasificación.109
En cuanto a los síntomas, estos se correlacionaron con los hallazgos radiográficos, después de un año de evaluación postoperatoria, los resultados indicaron que la mayoría de los pacientes que presentaron síntomas, obtuvieron una evaluación radiográfica de cicatrización insatisfactoria. Solo un caso de cicatrización completa presentó una fístula, posteriormente ésta se asoció con un conducto lateral sin tratamiento.62
Los síntomas subjetivos ocurrieron en solo el 2 a 3% de los casos con cicatrización completa, incompleta e incierta. Usualmente, los síntomas objetivos como fístula e inflamación intraoral, indicaban inflamación periapical.62
De acuerdo con Rud, Andreasen y Jensen 72 se puede esperar una tasa de éxito del 66% después de un año de realizar un procedimiento quirúrgico endodóntico; Zuolo, Ferreira y Gutmann 77 han reportado una tasa de 25 a 90%; mientras que Tobón et al.32 indicaron que podía variar entre 50 y 90%. La tasa de fracaso también ha sido reportada, la misma oscila entre el 2%,72,107 y 9 a 19%.31
Estas discrepancias se deben a la naturaleza del estudio, al tamaño de la muestra, a los materiales y métodos, al período de evaluación postoperatorio, a la edad del grupo estudiado y al criterio utilizado para determinar clínica y radiográficamente los parámetros de cicatrización.32,77,107
Zuolo, Ferreira y Gutmann 77 consideraron como exitosos a los casos que no presentaron signos o síntomas y radiográficamente evidenciaron cicatrización completa o incompleta (cicatriz); dudosos a los casos que aunque tenían ausencia de signos y síntomas, radiográficamente fueron clasificados como cicatrización incierta; y fracasados a aquellos casos que exhibían algún signo o síntoma y radiográficamente se catalogaron como cicatrización insatisfactoria.
Es relevante el hecho de que la mayoría de los casos exitosos o fracasados ocurrieron durante el primer año de evaluación postoperatoria.72,77,107 Por este motivo, todos los pacientes deberían asistir a los controles postoperatorios clínicos y radiográficos a los 6 meses y al año después de la intervención.37
Desde el punto de vista clínico, se recomienda no repetir la exploración de un campo quirúrgico previo cuando no hay signos y síntomas clínicos, como dolor, inflamación o drenaje de material purulento. En el paciente asintomático se indica la observación y control.38
Una vez, que el hueso se une con la cortical ósea, la apariencia radiográfica es normal. Aunque la reformación de la cortical ósea no es esencial para una apariencia sana.41
Discusión
La cicatrización después de un procedimiento quirúrgico endodóntico, es un proceso complejo que involucra a los tejidos blandos, duros y periapicales. La cicatrización depende del tipo de tejido lesionado y el tipo de daño que se realiza.11
Aunque por lo general el término cicatrización es utilizado para referirse a la curación de las heridas, existen diferentes tipos de cicatrización, donde se encuentran la reparación, regeneración, nueva inserción y reinserción.13-16,22
En la literatura existen innumerables artículos que se refieren a la cicatrización después de una cirugía periodontal, en contraste, las investigaciones disponibles de la cicatrización después de un procedimiento quirúrgico endodóntico, no son tan abundantes.
Muchos artículos relacionados con la cicatrización periodontal o de la piel después de un acto quirúrgico, se han adaptado a la cicatrización de los tejidos blandos y duros periapicales. De hecho, aunque los tejidos blandos bucales y la piel son prácticamente el mismo tipo de tejido, los tejidos blandos bucales cicatrizan más rápido que la piel.11
Harrison 11 refiere que es una equivocación pensar que la cicatrización de los tejidos blandos y óseos después de una cirugía periapical es la misma que ocurre después de un procedimiento de cirugía periodontal mucoperióstico.
La cirugía periodontal por lo general altera intencionalmente y remueve las enfermedades de los tejidos blandos y duros, dependiendo del tipo de procedimiento y colgajo que se realice la cicatrización será por primera o segunda intención. Mientras en la cirugía periapical, casi siempre se manipulan hueso de soporte y tejidos blandos sanos, por lo tanto la cicatrización de los tejidos mucoperiósticos, en la mayoría de los casos será por primera intención.11
Kakehashi 29 en 1965, demostró la relación que existe entre la inflamación pulpar y periapical y la infección bacteriana. La eliminación de las bacterias y sus componentes antigénicos del interior de los conductos radiculares, es el factor determinante para el predominio de los mediadores que favorecen la reparación y la disminución de los que propagan la inflamación.26
La presencia de una periodontitis apical, es un prerrequisito para realizar una cirugía endodóntica.31 La cirugía endodóntica se ejecuta para erradicar los irritantes provenientes del sistema de conductos radiculares y eliminar las causas potenciales de una inflamación periapical persistente32-34 y de esta forma permitir la reparación de los tejidos periapicales.34
La indicación de una cirugía periapical depende de cada caso en específico, aunque existen tres indicaciones que pueden ser adaptadas a una gran cantidad de situaciones clínicas, sin ser tan específicas.
La cirugía endodóntica se puede indicar cuando existe una gran posibilidad de fracasar con un tratamiento endodóntico no quirúrgico, si existe un fracaso como resultado de un tratamiento o retratamiento endodóntico y es imposible obtener un mejor resultado con la terapia convencional o cuando se requiere tomar una biopsia en o cerca del ápice radicular.27,35
Un procedimiento quirúrgico endodóntico requiere de una incisión que defina el perímetro del colgajo, lo que provoca una herida incisional; 11,19 posteriormente, el colgajo se debe reflejar completamente, incluyendo al periostio, para exponer la cortical o la ventana ósea, esto se conoce como herida diseccional.11,39
Finalmente, la remoción de hueso y la resección apical, crean una herida excisional que involucra al hueso, endostio, ligamento periodontal, cemento y dentina.11,12,40 Todos los tejidos involucrados en la herida excisional tienen capacidad de regeneración a excepción de la dentina.11,12 A diferencia de la herida incisional y diseccional, en la cicatrización de la herida excisional, los bordes no pueden ser reaproximados.40
La herida incisional cicatriza rápidamente y en cuatro fases prácticamente simultáneas; al parecer no existen diferencias en cuanto al tipo de colgajo realizado.11,19 Si los tejidos marginales se reposicionan adecuadamente, se puede observar una cicatrización completa del periodonto de protección después de 3 semanas de realizado el procedimiento.36
La cicatrización de la herida diseccional ocurre prácticamente de la misma forma que la herida incisional, pero a menor velocidad;11,39 a los 28 días, el periostio y la cresta ósea adquieren una apariencia microanatómica más normal. Tampoco se han encontrado diferencias durante la cicatrización de la herida diseccional al realizar colgajos triangulares o rectangulares submarginales.11,39
Aunque la secuencia exacta de los eventos que ocurren durante la cicatrización dentoalveolar apical, no se conocen todavía, al parecer las células ectomesenquimatosas indiferenciadas que provienen del ligamento periodontal y del endostio, se diferencian en fibroblastos, osteoblastos y cementoblastos. Que para la semana 16 después de realizada la cirugía, el aparato dentoalveolar apical se observa muy similar al normal.11
Algunos estudios han demostrado aposición de cemento durante la cicatrización dentoalveolar,31,36,43,44,48-50,55,60,63 otros indican la remoción de la capa de desecho ya que al parecer se puede acelerar este proceso si la raíz resecada se desmineraliza con ácido cítrico.11,12,23,25,31,41,43,45,46
En cuanto a la cicatrización ósea, el endostio juega un papel muy importante, el mismo provee las células ectomesenquimatosas indiferencias, las células osteoprogenitoras, los preosteoblastos y los osteoblastos. Ocho semanas después de realizada la cirugía, el endostio se puede observar idéntico al normal.11
La reparación completa de la herida excisional, excepto la cortical ósea, es apreciable en la semana 16. El período de tiempo exacto necesario para que la tabla cortical complete su reparación es todavía desconocido.11
Se ha determinado que si ambas corticales, vestibular y lingual, son destruidas por el proceso quirúrgico y/o patológico, la reparación deja una cicatriz que trae como consecuencia la persistencia en la radiografía de una imagen radiolúcida.7,51-53 Esto es debido a que usualmente no se completa la regeneración ósea y por lo tanto se desarrolla un denso tejido conjuntivo fibroso, lo que trae como consecuencia la formación de una cicatriz.11,38,51,52,55
Este fenómeno es común observarlo en los laterales superiores y no es un indicativo de fracaso endodóntico sino más bien otra forma de cicatrización.11,38,51,53,55,56
La cicatrización periapical y radicular después de una resección apical depende de la reacción del tejido conjuntivo que entra en contacto con las superficies expuestas.59
En la mayoría de los casos la resección radicular se ejecuta en presencia de una inflamación crónica periapical, la cual involucra al cemento y dentina. Al parecer, si los túbulos dentinarios se encuentran contaminados con bacterias no se podrá depositar nuevo cemento sobre esta superficie.59
Aunque existen estudios que han reportado cicatrización después de una resección apical,55,59-61 debido a que los fracasos endodónticos se relacionan con la inadecuada limpieza y conformación del sistema de conductos radiculares y la salida de irritantes hacia los tejidos periapicales,27,63 se ha recomendado la colocación de una obturación a retro en los dientes que requiere una resección apical.63
La apicectomía remueve hueso y cemento necrosados 52 y los irritantes provenientes del sistema de conductos radiculares,33,34 mientras que la obturación a retro apical tienen como objetivo, lograr un sellado impermeable que evite la salida hacia los tejidos perirradiculares de cualquier agente nocivo que no haya sido posible eliminar,63-65 facilitándose así el proceso de reparación.33,34,52
Hasta la fecha se han propuesto múltiples materiales de obturación a retro.33,47 Al parecer, la amalgama ofrece una tasa de éxito clínico baja, pobre capacidad de sellado, alto potencial de corrosión, sensibilidad a la humedad, pigmentación de los tejidos duros y blandos y toxicidad.63,70-74
En cambio el uso de IRM como material de obturación a retro ha demostrado éxito clínico74,77 y ha exhibido una aceptable reparación del tejido periapical.41,70,73 Por lo tanto se ha recomendado como material para obturar a retro cavidades en endodoncia.41,73,74 El SuperEBA también ha arrojado buenos resultados.70,74
Bajo condiciones ideales la cicatrización de la herida excisional debería culminar con la reformación del aparato de inserción apical 12,41,47 y aposición de cemento sobre el material de obturación a retro.31,47 Ésta es una característica que pocas veces se ha observado en los materiales convencionales de obturación a retro, pero ha sido detectada rutinariamente en los estudios con MTA.31,48-50
En cuanto al MTA, al parecer su capacidad de sellado y adaptación marginal es superior a la amalgama, IRM y SuperEBA 69 y aunque el mecanismo de formación del cemento sobre el MTA no está muy claro, al parecer, el MTA activa a los cementoblastos, lo que podría inducir la cementogénesis.80
No se pueden mencionar estudios a largo plazo, ya que el MTA tiene relativamente poco tiempo en el mercado. Aunque la gran mayoría de los estudio lo sugieren como un adecuado material de obturación a retro apical. Se recomienda la continuidad en los estudios del MTA, para evidenciar la efectividad del material, la estabilidad de sus propiedades su comportamiento y efecto biológico a largo plazo.69
El reimplante intencional es un procedimiento quirúrgico endodóntico que aunque no es considerado el tratamiento de elección para un diente con periodontitis apical, se considera como un tratamiento de último recurso cuando la terapéutica convencional, el retratamiento o la cirugía son imposibles.31,82,84
Los acontecimientos histológicos de la cicatrización después de reimplantar un diente comienzan desde el mismo momento de efectuarse la reimplantación. Dos semanas después de realizar un reimplante intencional, es casi imperceptible la línea de separación del ligamento periodontal y es frecuente observar a las fibras periodontales principales. Al transcurrir dos meses, las fibras principales se pueden apreciar normales en cantidad y orientación.85
La presencia y vitalidad del ligamento periodontal sobre la superficie radicular del diente reimplantado son decisivas para la cicatrización periodontal.84-87,92,93 Es por esto que se hacen muchos esfuerzos por mantener el ligamento periodontal vital para evitar así las consecuencias más indeseables que son, la resorción radicular externa y la anquilosis.84,86,87,93 Inclusive después de realizar una técnica cuidadosa, histológicamente la resorción inflamatoria 31,70,71,73,87,93 y la anquilosis 86,87,93 han sido complicaciones frecuentes.
La regeneración tisular guiada es un procedimiento de rutina en cirugía periodontal 98 y aunque no lo es en cirugía endodóntica, algunos autores la indican en los actos quirúrgicos endodónticos.31,32,37,56,57,98-100,102 Ya que puede aumentar las posibilidades de éxito del procedimiento.102
Los experimentos en animales, han demostrado que el uso de membranas reabsorbibles y no reabsorbibles producen regeneración del cemento, hueso alveolar y ligamento periodontal funcional.25,57,100
Pero no sólo se ha aplicado el principio de regeneración tisular guiada a los procedimientos quirúrgicos endodóntico, si no también se han colocado materiales de injerto en los defectos óseos.
Al parecer, los injertos óseos tienen un efecto regenerador en las grandes lesiones periapicales. Se cree, que el material implantado puede participar en el proceso osteogénico de una forma pasiva.104 Varios autores han reportado el aumento en la cementogénesis y osteogénesis en la zona del injerto.32,43,103-106
Los resultados obtenidos con la regeneración tisular guiada mejoran cuando la técnica se combina con injertos colocados en los defectos,25,32,98,102 lo que puede aumentar las posibilidades de éxito del procedimiento quirúrgico endodóntico.102
La literatura existente en general, ofrece muchas variaciones en los resultados obtenidos después de una cirugía endodóntica. Estas diferencias podrían depender del tipo de criterio aplicado para determinar la cicatrización.31,56,61,72,96,107
Es por esto que la evaluación debe ser cuidadosa ya que existen factores que pueden alterar los resultados, como por ejemplo: el criterio de cicatrización, el período de observación, la selección del caso, el método y tipo de material para la obturación a retro.31,56,61,72,96,107
Hasta ahora la determinación de la cicatrización debe basarse sólo en la evaluación clínica y radiográfica.37,54,61,96 Ya que desafortunadamente es imposible realizar un estudio histológico.61,62
El proceso de cicatrización completo, varía mucho de un individuo a otro; en algunos se hace evidente radiográficamente en cuestión de meses, mientras que en otros puede transcurrir un año o hasta 10 años para que se restablezca el patrón trabecular normal.37,38,52
Debido a la dificultad que existe para correlacionar los hallazgos radiográficos con el estado histológico periapical, el estudio de Andreasen y Rud 54 es una guía que trata de explicar la conexión que existe entre estos hallazgos. Así mismo, otra investigación dirigida por Rud, Andreasen y Jensen 62 propone una clasificación radiográfica muy útil y utilizada por otros autores para valorar la cicatrización periapical después de una cirugía endodóntica, mínimo después de un año postoperatorio.
Los criterios para valorar la condición periapical después de una cirugía endodóntica, estarán dirigidos a evaluar si la cicatrización fue satisfactoria, incierta o insatisfactoria. Para determinarla, se deben hacer controles postoperatorios a largo plazo.62
En cuanto a los síntomas, al parecer estos se correlacionan con los hallazgos radiográficos. Después de un año de evaluación postoperatoria, los resultados indicaron que la mayoría de los pacientes que presentaron síntomas, obtuvieron una evaluación radiográfica de cicatrización insatisfactoria.62
Es relevante el hecho de que la mayoría de los casos exitosos o fracasados ocurrieron durante el primer año de evaluación postoperatoria.72,77,107 Por este motivo, todos los pacientes deberían asistir a los controles postoperatorios clínicos y radiográficos a los 6 meses y al año después de la intervención.37
Conclusiones
1. El proceso de cicatrización involucra una serie de mecanismos complejos, que dependen del tipo de tejido y clase de herida realizada.
2. La cicatrización por primera intención se produce en los casos donde los bordes de la herida se encuentran próximos o en el mismo lugar que antes de producirse el daño, el resultado final de este tipo de cicatrización es la regeneración.
3. La cicatrización por segunda intención se efectúa cuando los bordes de la herida se encuentran separados, el resultado final de este tipo de cicatrización es la reparación.
4. La cicatrización de los tejidos mucoperiósticos es más rápida que la de los tejidos periapicales y radiculares.
5. La desmineralización con ácido cítrico de la superficie radicular resecada, remueve la capa de desecho y puede acelerar el proceso de cicatrización dentoalveolar.
6. Aunque no existe un material de obturación a retro apical ideal, el IRM y SuperEBA han exhibido una aceptable reparación del tejido periapical.
7. El MTA es un material de obturación a retro prometedor que en la mayoría de los estudios ha demostrado aposición de cemento sobre la superficie resecada, incluso sobre el material, pero se requieren más estudios a largo plazo para evaluar sus propiedades.
8. La presencia y vitalidad del ligamento periodontal sobre la superficie radicular de un diente reimplantado, son decisivas para la cicatrización periodontal.
9. Los procedimientos de regeneración tisular guiada e injertos óseos, pueden ser aplicados a los procedimientos quirúrgicos endodónticos.
10. El conocimiento del proceso de cicatrización y la evaluación clínica y radiográfica postoperatoria por varios años después de realizar el acto quirúrgico, es esencial para poder determinar si hubo o no cicatrización después de un procedimiento quirúrgico endodóntico.
11. No existe correlación exacta entre la condición histológica y los hallazgos clínicos y radiográficos. Pero por ahora son nuestra única herramienta de evaluación.
12. La cicatrización incompleta de una lesión periapical se evidencia radiográficamente como una imagen radiolúcida persistente, que en muchas ocasiones ésta es diagnosticada erróneamente como un fracaso quirúrgico endodóntico.
Referencias
1. Gómez M, Campos A. Periodoncio de protección: encía y unión dentogingival. En: Histología y embriología bucodental. Madrid. Editorial Médica Panamericana. 1999: 268-286.
2. Itoiz M, Carranza F. La encía. En: Carranza F, Newman M. editores. Periodontología clínica. México. McGraw-Hill Interamericana. 8va Edición. 1998: 14-32.
3. Gómez M, Campos A. Embriología general humana. En: Histología y embriología bucodental. Madrid. Editorial Médica Panamericana. 1999: 19-26.
4. Lindhe J, Karring T. Anatomía del periodonto. En: Lindhe J. editor. Periodontología clínica e implantología odontológica. Madrid. Editorial Médica Panamericana. 3era Edición. 2000: 19-68.
5. Gómez M, Campos A. Periodoncio de inserción: cemento, ligamento periodontal, y hueso alveolar. En: Histología y embriología bucodental. Madrid. Editorial Médica Panamericana. 1999: 298-324.
6. Carranza F, Ubios A. Las estructuras de soporte dentario. En: Carranza F, Newman M. editores. Periodontología clínica. México. McGraw-Hill Interamericana. 8va Edición. 1998: 33-55.
7. Harrison J. Anatomy and physiology of the periodontium. En: Gutmann J., Harrison J, editores. Surgical endodontics. Tokyo. Ishiyaku Euroamerica, Inc. 1994: 89-122.
8. Arens D, Adams W, DeCastro R. Consideraciones locales. En: Cirugía en endodoncia. Barcelona. Ediciones Doyma. 1984: 29-54.
9. Gartner L, Hiatt J. Cartílago y hueso. En: Texto atlas de histología. México. McGraw-Hill Interamericana. 2002: 127-151.
10. Robbins S, Cotran R, Kumar V, Collins T. Reparación de los tejidos: proliferación celular, fibrosis y curación de las heridas. En: Patología estructural y funcional. México. McGraw-Hill Interamericana. 6ta Edición. 2000: 95-120.
11. Harrison J. Surgical wound healing. En: Gutmann J, Harrison J, editores. Surgical endodontics. Tokyo. Ishiyaku Euroamerica, Inc. 1994: 300-337.
12. Craig K, Harrison J. Wound healing following demineralization of resected root ends in periradicular surgery. Journal of Endodontics. 1993; 19: 339-347.
13. Garrett S. Periodontal regeneration around natural teeth. Ann Periodontol 1996; 1: 621-66.
14. Mitchell R, Cotran R. Reparación: Regeneración celular, fibrosis y cicatrización de las heridas. En: Kumar V, Cotran R, Robbins S, editores. Patología humana. México. McGraw-Hill Interamericana. 6ta Edición. 1997: 51-64.
15. Hupp J. Wound repair. En: Peterson L, Ellis E, Hupp J, Tucker M, editores. Contemporary oral and maxillofacial surgery. St. Louis. Mosby. 3era Edición. 1998: 57-68.
16. Shafer W, Hine M, Levy B, Tomich C. Cicatrización de las lesiones bucales. En: Tratado de patología bucal. México. Nueva Editorial Interamericana. 4ta Edición. 1986: 614-635.
17. Diccionario terminológico de ciencias médicas. 11ra ed. Barcelona. Salvat, 1974: 192,869.
18. Diccionario ilustrado de odontología. Buenos Aires. Editorial Médica Panamericana S.A. 1992: 245, 1004, 1009.
19. Harrison J, Jurosky K. Wound healing in the tissue of the periodontium following periradicular surgery. I. The incisional wound. Journal of Endodontics. 1991; 17: 425-435.
20. Harrison J. Healing of surgical wounds in oral mucoperiostial tissues. Journal of Endodontics. 1991; 17: 401-408.
21. Ryan G, Majno G. Inflammation the healing phase. En: Inflammation. U.S.A. Upjohn. 1977:69-76.
22. Carranza F. Rationale for periodontal treatment. En: Newman M, Takei H y Carranza F. editores. Clinical Periodontology. Pennsylvania. W.B. Saunders Company. 9na Edición. 2002: 507-512.
23 Karring T, Lindhe J, Cortellini P. Tratamiento periodontal regenerativo. En: Lindhe J. editor. Periodontología clínica e implantología odontológica. Madrid. Editorial Médica Panamericana. 3era Edición. 2000: 604-654.
24. Collins T. Inflamación aguda y crónica. En: Robbins S, Cotran R, Kumar V, Collins T. editores. Patología estructural y funcional. México. McGraw-Hill Interamericana. 6ta Edición. 2000: 53-93.
25. Carranza F. Cirugía ósea reconstructiva. En: Carranza F, Newman M. editores. Periodontología clínica. México. McGraw-Hill Interamericana. 8va Edición. 1998: 668-686.
26. Canalda C, Fumarola J. Etiopatogenia de la enfermedad pulpar y periapical. En: Canalda C, Brau E. editores. Endodoncia. Barcelona. Masson. 2001: 42-55.
27. Siqueira J. Aetiology of root canal treatment failure: why well-treated teeth can fail. International Endodontic Journal. 2001; 34: 1-10.
28. Torabinejad M, Pitt Ford T. Root end filling materials: a review. Endodontic Dental Traumatology. 1996; 12: 161-178.
29. Kakehashi S, Stanley H, Fitzgerald R. The effect of surgical exposures of dental pulps in germ-free and conventional laboratory rats. Oral Surgery, Oral Medicine, Oral Pathology. 1965; 20: 340-349.
30. Stashenko P. Etiology and pathogenesis of pulpitis and apical periodontitis. En: Pitt Ford T, Orstavik D. editores. Essential endodontology. Paris. Blackwell Science. 1998: 42-67.
31. Pitt Ford T. Surgical treatment of apical periodontitis. En: Pitt Ford T, Orstavik D. editores. Essential endodontology. Paris. Blackwell Science. 1998: 278-307.
32. Tobón S, Arismendi J, Marín M, Mesa A, Valencia J. Comparison between a conventional technique and two bone regeneration techniques in periradicular surgery. International Endodontic Journal. 2002; 35: 635-641.
33. Jou Y, Pertl C. Is there a best retrograde filling material?. Dental Clinics of North America. 1997; 41: 555-561.
34. Ingle J, Cummings R, Frank A, Glick D, Rubistein R, Radman P. Cirugía endodóntica. En: Ingle J, Bakland L. editores. Endodoncia. México. McGraw-Hill Interamericana. 4ta Edición. 1996: 724-802.
35. Gutmann J. Historical, anatomical, and biological perspectives. En: Gutmann J, Harrison J, editores. Surgical endodontics. Tokyo. Ishiyaku Euroamerica, Inc. 1994: 3-41.
36. Dedolph T, Clark H. A histological study of mucoperiosteal flap healing. Journal of Oral Surgery. 1958; 16: 367-376.
37. Gay C. Cirugía periapical. En: Canalda C, Brau E. editores. Endodoncia. Barcelona. Masson. 2001: 300-321.
38. Arens D, Adams W, DeCastro R. Patología periapical de importancia endodóntica. En: Cirugía en endodoncia. Barcelona. Ediciones Doyma. 1984: 68-76.
39. Harrison J, Jurosky K. Wound healing in the tissue of the periodontium following periradicular surgery. II. The dissectional wound. Journal of Endodontics. 1991; 17: 544-552 .
40. Harrison J, Jurosky K. Wound healing in the tissue of the periodontium following periradicular surgery. III. The osseous excisional wound. Journal of Endodontics. 1992; 18: 76-81.
41. Harrison J, Johnson S. Excisional wound healing following the use of IRM as a root-end filling material. Journal of Endodontics. 1997; 23: 19-27.
42. Stahl S, Tarnow D. Root resorption leading to linkage of dentinal collagen and gingival fibers?. Journal of Clinical Periodontology. 1985; 12: 399-404.
43. Bowers G, Schallhorn R, Mellonig J. Histologic evaluation of new attachment in human intrabony defects. Journal of Periodontology. 1982; 53: 509-514.
44. Andreasen J. Cementum repair after apicoectomy in humans. Acta Odontológica Scandinava. 1973; 31: 211-221.
45. Polson A, Ladenheim S, Hanes P. Cell and fiber attachment to demineralized dentin from periodontitis-affected root surfaces. Journal of Periodontology. 1986; 57: 235-246.
46. Proye M, Polson A. Repair in different zones of the periodontium after tooth reimplantation. Journal of Periodontology. 1982; 53: 379-389.
47. Keiser K, Johnson C, Tipton D. Cytotoxicity of mineral trioxide aggregate using human periodontal ligament fibroblasts. Journal of Endodontic. 2000; 26: 288-291.
48. Torabinejad M, Pitt Ford T, McKendry D, Abedi H, Miller D, Kariyawasam S. Histologic assessment of mineral trioxide aggregate as a root-end filling in monkeys. Journal of Endodontics. 1997; 23: 225-228.
49. Torabinejad M, Hong C, Lee S, Monsef M, Pitt Ford T. Investigation of mineral trioxide aggregate for root-end filling in dogs. Journal of Endodontics. 1995; 21: 603-608.
50. Koh E, McDonald F, Pitt Ford T, Torabinejad M. Cellular response to mineral trioxide aggregate. Journal of Endodontic. 1998; 24: 543-547.
51. Rud J, Andreasen J, Jensen M. A multivariate analysis of the influence of various factors upon healing after endodontic surgery. International Journal of Oral Surgery. 1972; 1: 258-271.
52. Grossman L. Apicectomía. En: Práctica endodóntica. Buenos Aires. Mundi S.A.I.C y F. 3era Edición. 1973: 318-345.
53. Molven O, Halse A, Grung B. Incomplete healing (scar tissue) after periapical surgery &endash; radiographic findings 8 to 12 years alter treatment. Journal of Endodontics. 1996; 22: 264-268.
54. Andreasen J, Rud J. Correlation between histology and radiography in the assessment of healing after endodontic surgery. International Journal of Oral Surgery. 1972; 1: 161-173.
55. Andreasen J, Rud J. Modes of healing histologically after endodontic surgery in 70 cases. International Journal of Oral Surgery. 1972; 1: 148-160.
56. Pecora G, Kim S, Celletti R, Davarpanah M. The guide tissue regeneration principle in endodontic surgery: one year postoperative result of large periapical lesions. International Endodontic Journal. 1995; 28: 41-46.
57. Baek S, Kim S. Bone repair of experimentally induce through-and-through defects by Gore-Tex, Guidor, and Vicryl in ferrets: A pilot study. Oral Surgery, Oral Medicine, Oral Pathology. 2001; 91: 710-714.
58. Lang N, Becker W, Karring T. Formación de hueso alveolar. En: Lindhe J. editor. Periodontología clínica e implantología odontológica. Madrid. Editorial Médica Panamericana. 3era Edición. 2000: 916-948.
59. Coolidge E. Root resection as a cure for chronic periapical infection: a histologic report of a case showing complete repair. Journal of American Dental Association. 1930; 17: 239-249.
60. Svejda J, Brazda O. Scanning electron microscopic examination of root after apicoectomy. Journal of Oral Pathology. 1978; 7: 162-172.
61. Hirsch J, Ahlström U, Henrikson P, Heyden G, Peterson L. Periapical surgery. International Journal of Oral Surgery. 1979; 8: 173-185.
62. Rud J, Andreasen J, Jensen M. Radiographic criteria for the assessment of healing after endodontic surgery. International Journal of Oral Surgery. 1972; 1: 195-214.
63. Torabinejad M, Higa R, McKendry D, Pitt Ford T. Dye leakage of tour root end filling materials: effects of blood contamination. Journal of Endodontic. 1994; 20: 159-163.
64. Carr G. Preparación ultrasónica del extremo radicular. Clínicas Odontológicas de Norte América. 1997; 3: 611-625.
65. Arens D, Torabinejad M, Chivian N, Rubinstein R. Retrograde instrumentation: root end preparation. En: Practical lessons in endodontic surgery. Illinois. Quintessence Books. 1998: 105-116.
66. Torabinejad M, Hong C, McDonald F, Pitt Ford T. Physical and chemical properties of a new root-end filling material. Journal of Endodontic. 1995; 21: 349-353.
67. Torabinejad M, Rastegar A, Kettering J, Pitt Ford T. Bacterial leakage of mineral trioxide aggregate as a root-end filling material. Journal of Endodontic. 1995; 21: 109-112.
68. Torabinejad M, Hong C, Pitt Ford T, Kettering J. Cytotoxicity of four root end filling materials. Journal of Endodontic. 1995; 21: 489-492.
69. Di Giuseppe E. Aplicación clínica del agregado trióxido mineral (MTA) en endodoncia. Caracas. Universidad Central de Venezuela. 1999.
70. Pitt Ford T, Andreasen J, Dorn S, Kariyawasam S. Effect of various zinc oxide materials as root-end fillings on healing after replantation. International Endodontic Journal. 1995; 28: 273-278.
71. Pitt Ford T, Andreasen J, Dorn S, Kariyawasam S. Effect of various sealers with gutta-percha as root-end fillings on healing after replantation. Endodontic and Dental Traumatology. 1996; 12: 33-37.
72. Rud J, Andreasen J, Jensen M. A follow-up study of 1.000 cases treated by endodontic surgery. International Journal of Oral Surgery. 1972; 1: 215-228.
73. Pitt Ford T, Andreasen J, Dorn S, Kariyawasam S. Effect of IRM root-end fillings on healing after replantation. Journal of Endodontics. 1994; 20: 381-385.
74. Dorn S, Gartner A. Retrograde filling materials: a retrospective success-failure study of amalgam, EBA and IRM. Journal of Endodontics.1990; 16: 391-393.
75. Andreasen J. Reimplantación intencional. En: Reimplantación y transplante en odontología. Atlas. Buenos Aires. Editorial Médica Panamericana S.A. 1992: 99-109.
76. Emmertsen E, Andreasen J. Replantation of extracted molars. A radiographic and histological study. Acta Odontológica Scandinava. 1966; 24: 327-346.
77. Zuolo M, Ferreira M, Gutmann J. Prognosis in periradicular surgery: a clinical prospective study. International Endodontic Journal. 2000; 33: 91-98.
78. Rapp E, Brown C, Newton C. An analysis of success and failure of apicoectomies. Journal of Endodontics. 1991; 17: 508-512.
79. Lustmann J, Friedman S, Shaharabany V. Relation of pre- and intraoperative factors to prognosis of posterior apical surgery. Journal of Endodontics. 1991; 17: 239-241.
80. Torabinejad M, Watson T, Pitt Ford T. Ability of a mineral trioxide aggregate as a retrograde root filling material. Journal of Endodontic. 1993; 19: 591-595.
81. American Association of Endodontists. Glossary Contemporary Terminology for Endodontics. Chicago. 5ta Edición. 1994: 1-25.
82. Aqrabawi J. Five-year follow-up of successful intentional replantation. Dental Update. 1999; 26: 388-390.
83. Grossman L. Intentional replantation of teeth. Journal of American Dental Association. 1966; 72: 1111-1118.
84. Dryden J, Arens D. Reimplantación intencional: Una alternativa viable para casos seleccionados. Clínicas Odontológicas de Norteamérica. 1994; 2:299-325.
85. Andreasen J. Anatomía quirúrgica y cicatrización de heridas. En: Reimplantación y transplante en odontología. Atlas. Buenos Aires. Editorial Médica Panamericana S.A. 1992: 15-56.
86. Andreasen J. Periodontal healing after replantation and autotransplantation of incisor in monkeys. International Journal of Oral Surgery. 1981; 10: 54-61.
87. Andreasen J. Effect of extra-alveolar period and storage media upon periodontal and pulpal healing after replantation of mature permanent incisor in monkeys. International Journal of Oral Surgery. 1981; 10: 43-53.
88. Pettini F, Pettini P. Root resorption of replanted teeth: an SEM study. Endodontic Dental Traumatology. 1998; 14: 144-149.
89. Andreasen J. Relationship between surface and inflammatory resorption and changes in the pulp alter replantation of permanent incisor in monkeys. Journal of Endodontics. 1981; 7: 294-301.
90. Andreasen J. Relationship between surface and inflammatory resorption and changes in the pulp alter replantation of permanent incisor in monkeys. Journal of Endodontics. 1982; 8: 426-427.
91. Trope M, Hupp J. The role of the socket in the periodontal healing of replanted dogs` teeth stored in ViaSpan for extended periods. Endodontic Dental Traumatology. 1997; 13: 171-175.
92. Oswald R, Harrington G, Van Hassel H. A postreplantation evaluation of air-dried and saliva-stored avulsed teeth. Journal of Endodontics. 1980; 6: 546-551.
93. Andreasen J, Reinholdt J, Riis I, Dybdahl R, Söder P, Otteskog P. Periodontal and pulpal healing of monkey incisor preserved in tissue culture before replantation. International Journal of Oral Surgery. 1978; 7: 104-112.
94. Oswald R, Harrington G, Van Hassel H. Replantation 1. The role of the socket. Journal of Endodontics. 1980; 6: 479-484.
95. Agnew R, Fong C. Histologic studies on experimental transplantation of teeth. Oral Surgery. 1956; 9:18-920.
96. Gutmann J. Endodoncia quirúrgica. En: Pitt Ford T. editor. Endodoncia en la práctica clínica. México. McGraw-Hill Interamericana. 4ta Edición. 1999: 154-190.
97. Nasjleti C, Caffesse R, Castelli W, Hoke J. Healing after tooth reimplantation in monkeys. Oral Surgery. 1975; 39: 361-375.
98. Rankow H, Krasner P. Endodontic applications of guided tissue regeneration in endodontic surgery. Journal of Endodontics. 1996; 22: 34-43.
99. Aguirre A, Llorente A, Eguizabal J, Martínez-Conde R, Cundin E, Santamaria J. Guided tissue regeneration procedure applied to the treatment of endodontic-periodontal disease: Analysis of a case. Quintessence International. 1997; 28: 87-91.
100. Douthitt J, Gutmann J, Witherspoon D. Histologic assessment of healing after the use of a bioresorbable membrane in the management of buccal bone loss concomitant periradicular surgery. Journal of Endodontics. 2001; 27: 404-410.
101. Maguire H, Torabinejad M, McKendry D, McMillan P, Simon J. Effects of resorbable membrane placement and human osteogenic protein-1 hard tissue healing alter periradicular surgery in cats. Journal of Endodontics. 1998; 24: 720-725.
102. Uchin R. Use of a bioresorbable guided tissue membrane as an adjunct to bony regeneration in cases requiring endodontic surgical intervention. Journal of Endodontics. 1996; 22: 94-96.
103. Dragoo M, Sullivan H. A clinical and histological evaluation of autogenous iliac bone grafts in humans: Part I. Wound healing 2 to 8 months. Journal of Periodontology. 1973; 44: 599-613.
104. Boyne P, Miller C. The effects of osseous implant materials on regeneration of alveolar cortex. Oral Surgery, Oral Medicine, Oral Pathology. 1961; 14: 369-378.
105. Hiatt W, Schallhorn R, Aaronian A. The induction of new bone and cementum formation. IV. Microscopic examination of the periodontium following human bone and marrow allograft, autograft and nongraft periodontal regenerative procedures. Journal of Periodontology. 1978; 49: 495-512.
106. Froum S, Thaler R, Scopp I, Stahl S. Osseous autografts. II. Histologic responses to osseous coagulum-bone blend grafts. Journal of Periodontology. 1975; 46: 656-661.
107. Grung B, Molven O, Halse A. Periapical surgery in a Norwegian county hospital: follow-up findings of 477 teeth. Journal of Endodontics. 1990; 16: 411-417.
108. Rud J, Andreasen J. A study of failures after endodontic surgery by radiographic, histologic and stereomicroscopic methods. International Journal of Oral Surgery. 1972; 1: 311-328.
109. Jesslen P, Zetterqvist I, Heimdahl A. Long-term result of amalgam versus glass ionomer cement as apical sealant after apicectomy. Oral Surgery, Oral Medicine, Oral Pathology, Oral Radiology and Endodontics. 1995; 79: 101-103.
Invitados Anteriores y sus Trabajos
![]()
¿Comentarios? carlosboveda@carlosboveda.com.
![]()
![]()
![]() Carlos
Bóveda
Z.v
Noviembre 2003
Carlos
Bóveda
Z.v
Noviembre 2003